
下列关于碱金属元素和卤素的说法中,错误的是
A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强
C.钾与水的反应比钠与水的反应更剧烈
D.溴单质与水的反应比氯单质与水的反应更剧烈
科目:高中化学 来源:2015-2016学年河北省唐山市高一下学期期中文科化学试卷(解析版) 题型:选择题
下列说法正确的是
①参加反应的物质的性质是影响化学反应速率的主要因素
②光是影响某些化学反应速率的外界条件之一
③决定化学反应速率的主要因素是浓度
④不管什么反应,增大浓度、加热、加压、使用催化剂都可以加快反应速率
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷(解析版) 题型:选择题
下列有关第ⅦA族元素的单质和化合物性质说法正确的是
A.还原性:HF>HCl>HBr>HI B.稳定性:HF<HCl<HBr<HI
C.从F2到I2,颜色逐渐加深 D.与氢气化合由易到难:I2>Br2> Cl2>F2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷(解析版) 题型:选择题
向四个体积相同的密闭容器中分别充入一定量的SO2和O2, 开始反应时, 按正反应速率由大到小的顺序排列, 正确的是
①500 ℃, 10 mol SO2和5 mol O2反应
②500 ℃, 用V2O5作催化剂, 10 mol SO2和5 mol O2反应;
③450 ℃, 8 mol SO2和5 mol O2反应
④500 ℃, 8 mol SO2和5 mol O2反应。
A.①②③④ B.②①③④ C.②①④③ D.④③②①
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市大名等四县高二下学期期中联考化学试卷(解析版) 题型:填空题
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①下列情形不能说明该反应已达到平衡状态的是 (填序号).
A.每消耗1mol CO的同时生成2molH2 B.混合气体总物质的量不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.生成CH3OH的速率与消耗CO的速率相等
②CO的平衡转化率(α)与温度、压强的关系如下图所示。
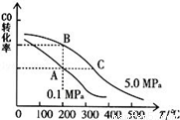
A、B两点的平衡常数K(A) K(B)(填“>”、“=”或“<”).
③某温度下,将2.0mol CO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,
CO的转化率= ,此温度下的平衡常数K= (保留两位有效数字).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市大名等四县高二下学期期中联考化学试卷(解析版) 题型:选择题
X、Y、Z、M为原子序数依次增大的4种短周期元素。已知X、Y、Z是同周期的相邻元素,M原子的核外电子数是Z原子最外层电子数的2倍,Y与其同主族的短周期元素可形成一种常见的气体。下列说法正确的是( )
A. 原子半径:M>X>Y>Z B. 对应氢化物的沸点: M>Z>Y>X
C. 对应氢化物的稳定性: Z>X>Y>M D. XY2与MY2溶于水都能得到对应的酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下学期期中考试化学试卷(解析版) 题型:填空题
有X、Y、Z、T、U五种短周期元素。X、Y、Z三元素在周期表中的位置如下所示,三元素的原子序数之和是41。X和T的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物。U单质在Z单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红。
X | |
Y | Z |
(1)各元素的符号是:Z________,T________
(2)Y原子的结构示意图为____________________,U2X的电子式
(3)YX2和U2Y反应的化学方程式为____________________________,其中氧化剂是____________,被氧化的元素是____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高二下学期期中考试化学试卷(解析版) 题型:填空题
现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其他五种元素都是短周期元素。X、Y、E三种元素组成的化合物是实验室常用燃料,也是一种家庭常见饮品的主要成分。取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体。G2E是红色固体。请回答下列问题:
(1)写出基态G原子电子排布式: ;Y、Z、E、F、G的第一电离能由小到大的顺序为 (用元素符号表示)。
(2)X、Y、Z形成3原子分子M,每个原子价层电子均达到稳定结构。M分子的结构式为 。1molM含 键数目为 。
键数目为 。
(3)根据价层电子对互斥理论(VESPR)推测:ZE2—的立体构型为 ,YE32—的中心原子杂化类型为 。
(4)Y、E、Z分别与X形成的简单化合物沸点由高到底的顺序为 (用化学式表示) 。
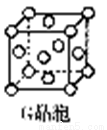
(5)G晶胞结构如图所示。已知立方体的棱长为apm,G 晶体密度为bg·cm-3,则阿伏加德罗常数NA= (用含a、b的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com