
���� ��1������һ�е�����NaOHʹ��Һ��pH=12ʱ����� KspMn��OH��2=2.06��10-13����������Ũ�ȣ�
��2�����ܽ�������ƿ��ע��20.00mLˮ�����ٷֱ����1mL 0.1mol•L-1MnSO4��Һ��3mL NaOH��KI�Ļ����Һ����ַ�Ӧ����ʱ������Ӧ�Ļ�ѧ����ʽΪ��Mn2++2OH-�TMn��OH��2�� 2Mn��OH��2+O2�T2MnO��OH��2��������������м���1.5mLŨ���ᣬ��ַ�Ӧ���Ƴ�����ȫ�ܽ⣬��ʱ��Һ�ʻ�ɫ��˵��MnO��OH��2 ����KI���ɵⵥ�ʣ�
��3���ɻ�ѧ����ʽ��֪��O2〜4Na2S2O3������õ���������
��� �⣺��1������NaOHʹ��Һ��pH=12ʱ��c��H+��=10-12mol/L��c��OH-��=10-2mol/L����� KspMn��OH��2=2.06��10-13���㣬KspMn��OH��2=c��Mn2+��c2��OH-��=2.06��10-13����õ���c��Mn2+��=2.06��10-9 ��
�ʴ�Ϊ��2.06��10-9��
��2�����ܽ�������ƿ��ע��20.00mLˮ�����ٷֱ����1mL 0.1mol•L-1MnSO4��Һ��3mL NaOH��KI�Ļ����Һ����ַ�Ӧ����ʱ������Ӧ�Ļ�ѧ����ʽΪ��Mn2++2OH-�TMn��OH��2�� 2Mn��OH��2+O2�T2MnO��OH��2��������������м���1.5mLŨ���ᣬ��ַ�Ӧ���Ƴ�����ȫ�ܽ⣬��ʱ��Һ�ʻ�ɫ��˵��MnO��OH��2 ����KI���ɵⵥ�ʣ���Ӧ�Ļ�ѧ����ʽΪ��MnO��OH��2+2H2SO4+2KI=MnSO4+K2SO4+I2+3H2O��
�ʴ�Ϊ��MnO��OH��2+2H2SO4+2KI=MnSO4+K2SO4+I2+3H2O��
��3���ɻ�ѧ����ʽ��֪��O2〜4Na2S2O3��
n��O2��=$\frac{1}{4}$��0.005mol•L-1��3.60��10-3L=4.5��10-6mol
�ܽ����ĺ����T4.5��10-6mol��16g/mol��$\frac{4.5��1{0}^{-6}mol��32g/mol}{0.02L}$=7.2g/L=7.2 mg•L-1��
�𣺸�ˮ�����ܽ����ĺ���Ϊ7.2 mg•L-1��
���� ���⿼����������ɡ����ʺ����IJⶨ���ζ�ʵ����̵�����Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Y����������Ԫ�ؾ����γ��������ֻ��������Ԫ����ɣ� | |
| B�� | ԭ�Ӱ뾶�ɴ�С���е�˳���ǣ�R��W��Z��Y��X | |
| C�� | ��Z��Y�γɵ��������ӻ��������������ӵĸ����Ⱦ�Ϊ2��1 | |
| D�� | Y��Z��W����Ԫ����ɻ������ˮ��Һһ���Լ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����Һ | B�� | ����������Һ | C�� | ������Һ | D�� | ����ʯ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2SO4[H2SO4] | B�� | KBr[H2O] | C�� | ����[HCl] | D�� | Cu��NO3��2[Cu��OH��2] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na2O2��s��+2CO2�� s��=2Na2CO3��s��+O2��g����H��-452 kJ/mol | |
| B�� | CO��ȼ����Ϊ283 kJ | |
| C�� | 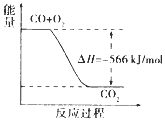 ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ | |
| D�� | CO��g����Na2O2��s����Ӧ�ų�509kJ����ʱ������ת����Ϊ6.02��l023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 136g���ڵ�KHSO4�к���2NA�������� | |
| B�� | 40gH218O��40gD2O��������������Ϊ20NA | |
| C�� | 1molFe�ֱ���������ϡ�����ϡ���ᷴӦת�Ƶ�������Ϊ2NA | |
| D�� | ��״���£�22.4LNO��11.2LO2��Ϻ�����ķ�������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
 |  |  |  |
| ���к��� | ���ˮ�еμ�FeCl3������Һ���ڼ��ȵ����ֺ��ɫ���������Ƶ�Fe��OH��3���� | ʵ����ԭ������ | ����CO2�е�HCl���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ճ������г���75%���Ҵ���Һ��ɱ������ | |
| B�� | ���õ�����Һ�����ʳ�����Ƿ� | |
| C�� | ���ͷ�����Ҫ����̼���ƣ���ʹ���Ƴ��ĸ�����ɶ�� | |
| D�� | ҽԺ�г���̼�ᱵ��Ϊ������Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ | B�� | ���� | C�� | ���� | D�� | ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com