
| A、由反应可确定:氧化性HClO4>HClO |
| B、变蓝的淀粉碘化钾试纸褪色是因为可能发生了:5C12+I2+6H2O=12H++10Cl-+2IO3- |
| C、若氯酸分解所得混合气体,lmol混合气体质量为47.6g,则反应方程式可表示:26HClO3=15O2↑+8C12↑+10HClO4+8H2O |
| D、若化学计量数a=8,b=3,则该反应转移电子数为10e- |
| n(O2)×32g/mol+n(Cl2)×71g/mol |
| n(O2)+n(Cl2) |


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
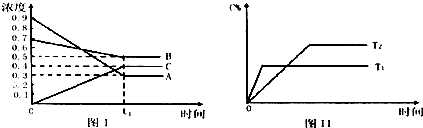
| A、在时间为t1时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B、在时间为t1时,保持温度和压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、其它条件不变,T℃时由0.6 mol/LA、0.6mol/LB、0.2mol/LC开始反应,达到平衡后C的浓度仍为0.4mol/L |
| D、其它条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所有氧化还原反应中,氧化剂的氧化性一定强于氧化产物的氧化性 |
| B、根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 |
| C、用酿造C2H5OH作燃料,不会增加大气中CO2含量 |
| D、氟氯烃含量是空气质量报告的主要项目之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.8g熔融KHSO4与3.9g Na202阴离子数目相同 |
B、某金属阳离子的结构为: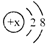 与Cl-形成的强电解质都是离子化合物 与Cl-形成的强电解质都是离子化合物 |
C、二硫化碳是直线型的分子,其电子式是: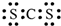 |
| D、因为氯、溴、碘非金属性逐渐减弱,所以其氢化物酸性HCl>HBr>HI |
查看答案和解析>>
科目:高中化学 来源: 题型:

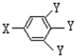 (其中:-X、-Y均为官能团)
(其中:-X、-Y均为官能团)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com