

| A. | ②④ | B. | ②③⑤ | C. | ①②③⑤ | D. | ①②④ |
科目:高中化学 来源: 题型:选择题
 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电反应的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列关于此电池说法正确的是( )
如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电反应的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列关于此电池说法正确的是( )| A. | 充电过程中,当0.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子 | |
| B. | 电池放电时,负极反应为:3NaBr一2e-═NaBr3+2Na+ | |
| C. | 充电过程中钠离子从右到左通过离子交换膜 | |
| D. | 放电过程中钠离子从左到右通过离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
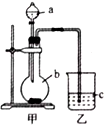 某同学想通过比较元素的最高价氧化物对应的水化物的酸性强弱来证明硫和碳的得电子能力强弱,设计了如图所示装置进行探究.
某同学想通过比较元素的最高价氧化物对应的水化物的酸性强弱来证明硫和碳的得电子能力强弱,设计了如图所示装置进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 观察焰色反应实验为黄色火焰,则可证明该溶液中含有Na+ | |
| B. | 金属单质导电与电解质溶液导电原因是一样的 | |
| C. | 常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏贮运浓硫酸 | |
| D. | 可用Na与MgCl2溶液反应制Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系(可能有部分生成物未标出),请回答下列问题:
单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系(可能有部分生成物未标出),请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 63Li和73Li是同一种核素 | B. | 63Li和73Li的中子数相同 | ||
| C. | 63Li和73Li的电子数相差1 | D. | 63Li和73Li的质子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、CH4在负极失去电子,发生氧化反应 | |
| B. | 从产物推断,两种燃料电池的氧化剂均为O2 | |
| C. | 燃料电池将化学能直接转变为电能,能量转化率高 | |
| D. | 分别将1 mol H2与1 mol CH4做燃料电池的燃料,转移的电子一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 产品标准 | GZ5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com