
分析 由相同元素组成的二元化合物A和B,A溶于水可得只含单一溶质C的弱酸性溶液,C有很强的氧化性,可用做漂白剂和消毒剂,则A为Cl2O,C为HClO,且A、B相对分子质量相差19.5,则B为ClO2.ClO2遇热水生成HClO、气体单质D和氧气,D为氯气;
(1)A中所有原子均满足8电子稳定结构,O原子与2个Cl分别形成1对共用电子对;
(2)ClO2遇热水生成HClO、氯气和氧气,配平书写方程式;
(3)一定条件下,氯气与潮湿的Na2CO3反应只生成气体Cl2O和两种钠盐,两种钠盐只能为NaCl、NaHCO3;
(4)破碎后使用,生成的HClO直接被Na2SO3还原,降低杀菌消毒效果;
(5)甲的粉末在足量的空气中充分灼烧,得到能使品红褪色的气体为SO2,计算二氧化硫物质的量,CuO、Fe2O3全部溶于稀盐酸后,加入铜粉充分反应,发生反应为:2Fe3++Cu=2Fe2++Cu2+,有5.0g-1.8g=3.2gCu参加了反应,根据方程式计算Fe元素物质的量,由Fe元素守恒计算氧化铁物质的量,可得CuO物质的量,根据质量守恒判断是否含有氧元素,结合原子数目之比确定化合物甲的化学式.
解答 解:由相同元素组成的二元化合物A和B,A溶于水可得只含单一溶质C的弱酸性溶液,C有很强的氧化性,可用做漂白剂和消毒剂,则A为Cl2O,C为HClO,且A、B相对分子质量相差19.5,则B为ClO2.ClO2遇热水生成HClO、气体单质D和氧气,D为氯气;
(1)A中所有原子均满足8电子稳定结构,O原子与2个Cl分别形成1对共用电子对,结构式为Cl-O-Cl,
故答案为:Cl-O-Cl;
(2)ClO2遇热水生成HClO、氯气和氧气,反应方程式为:6ClO2+2H2O═Cl2+5O2+4HClO,
故答案为:6ClO2+2H2O═Cl2+5O2+4HClO;
(3)一定条件下,氯气与潮湿的Na2CO3反应只生成气体Cl2O和两种钠盐,两种钠盐只能为NaCl、NaHCO3,反应方程式为:2Cl2+2Na2CO3+H2O═Cl2O+2NaHCO3+2NaCl,
故答案为:2Cl2+2Na2CO3+H2O═Cl2O+2NaHCO3+2NaCl;
(4)破碎后使用,生成的HClO直接被Na2SO3还原,降低杀菌消毒效果,不能先破碎后使用,
故答案为:不能;破碎后使用,生成的HClO直接被Na2SO3还原,降低杀菌消毒效果;
(5)甲的粉末在足量的空气中充分灼烧,得到能使品红褪色的气体为SO2,n(S)=n(SO2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,
CuO、Fe2O3全部溶于稀盐酸后,加入铜粉充分反应,发生反应为:2Fe3++Cu=2Fe2++Cu2+,有5.0g-1.8g=3.2gCu参加了反应,即参加反应的Cu的物质的量为$\frac{3.2g}{64g/mol}$=0.05mol,则n(Fe)=n(Fe3+)=2n(Cu)=2×0.05mol=0.1mol,
固体乙中m(CuO)=16g-0.1mol×$\frac{1}{2}$×160g/mol=8g,则n(Cu)=n(CuO)=$\frac{8g}{80g/mol}$=0.1mol,
m(S)+m(Fe)+m(Cu)=0.2mol×32g/mol+0.1mol×56g/mol+0.1mol×64g/mol=18.4g,等于甲的质量,故甲中不含元素,
综上所述,甲中n(Cu):n(Fe):n(S)=0.1mol:0.1mol:0.2mol=1:1:2,
因此化合物甲的化学式是CuFeS2,
故答案为:CuFeS2.
点评 本题考查无机物的推断,侧重考查学生对知识的综合应用及计算推理能力,需要学生具备扎实的基础,难度较大.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:选择题
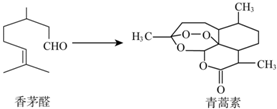 中国科学家屠呦呦因为创制了新型抗疟疾-青蒿素,获得2015年诺贝尔奖.青蒿素可由香茅醛为原料制取,下列说法错误的是( )
中国科学家屠呦呦因为创制了新型抗疟疾-青蒿素,获得2015年诺贝尔奖.青蒿素可由香茅醛为原料制取,下列说法错误的是( )| A. | 香茅醛能使Br2的CCl4溶液褪色 | B. | 青蒿素分子式为C15H22O5 | ||
| C. | 青蒿素含有和H2O2相同的过氧键 | D. | 青蒿素能与氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过渡元素全部都是副族元素 | |
| B. | 短周期共有32种元素 | |
| C. | 元素周期表共七个横行代表七个周期,18个纵行代表18个族 | |
| D. | 主族元素原子的最外层电子数等于该元素所属的族序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
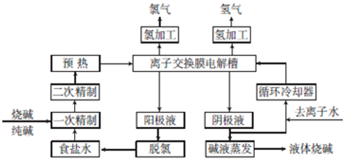
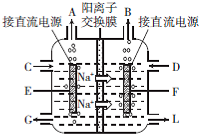
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>B>C>D | B. | D>B>A>C | C. | B>A>C>D | D. | C>B>A>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ICl中I显-1价 | |
| B. | HI是反应的中间产物 | |
| C. | 总反应速率的快慢主要由反应②决定 | |
| D. | 总反应的热化学方程式为H2(g)+2ICl(s)=I2(s)+2HCl(g)△H=-109kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 气态氢化物的稳定性:Z>W | |
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com