
下列有关实验正确的是
A.甲烷中混有的乙烯可通过酸性高锰酸钾溶液来除去
B.除去乙酸乙酯中的乙酸,先加入饱和Na2CO3溶液再分液
C.加稀硫酸的淀粉水解实验的溶液中,加入新制的氢氧化铜并加热以确定水解产物葡萄糖
D.用水能鉴别乙醇、甘油和四氯化碳
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(全国1卷参考版) 题型:选择题
下列实验操作能达到实验目的的是
A.用长颈漏斗分离出乙酸与乙醇反应的产物
B.用向上排空气法收集铜粉与稀硝酸反应产生的NO
C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释
D.将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市十校联合高二下期中化学试卷(解析版) 题型:选择题
某有机物分子式C3H6O2可与新制的Cu(OH)2在加热时反应生成砖红色沉淀,经检测核磁共振氢谱中有三个共振峰,面积比为3∶2∶1,该有机物的结构简式是( )


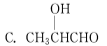
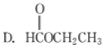
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:填空题
常用于制备食品香料的有机化合物A,其相对分子质量为120,A燃烧只生成二氧化碳和水。A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,且测得A与乙醇完全酯化所得有机产物B的相对分子质量为176。请回答下列问题:
(1)A的分子式为 。
(2)B的结构简式 。
(3)A与乙酸发生酯化反应的化学方程式 。
(4)由丙烯经过六个步骤可以合成有机化合物A,流程如下:
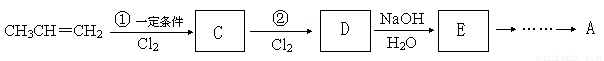
若C的分子式为C3H5Cl,D的分子式为C3H5Cl3,则①的反应类型为 。
D→E反应的化学方程式为 。
请补充完成E→A的反应流程 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
分子式为C5H10O2的有机物X,在酸性条件能够发生水解反应生成相对分子质量相等的两种有机物,符合条件的有机物X有
A.2种 B.4种 C.9种 D.13种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.丁烷的球棍模型 
B.乙烯的比例模型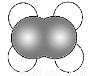
C.乙醛的结构简式CH3COH
D.键线式 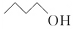 表示的有机物名称为1-戊醇
表示的有机物名称为1-戊醇
查看答案和解析>>
科目:高中化学 来源:2016届广东省佛山市高三4月二模理综化学试卷(解析版) 题型:填空题
请你利用所学反应原理知识解决下列问题:
I、(1)若已知两个反应:①C(s)+2H2(g)=CH4(g) ΔH1= a kJ·mol-1 ;②C(s)+ 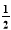 O2(g)=CO(g) ΔH2= b kJ·mol-1 ;
O2(g)=CO(g) ΔH2= b kJ·mol-1 ;
则2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH= (用含a、b的式子表示);
(2)碱性镁锰干电池是新开发的一种干电池,比普通锌锰干电池具有更加优越的性能,具有较大应用前景,其工作时总反应为:Mg+2MnO2+H2O=Mg(OH)2+Mn2O3;则工作时,正极发生 反应(填反应类型),写出负极的电极反应式: ;
(3)在一定温度下1 L的密闭容器放入足量草酸钙(固体所占体积忽略不计)发生反应:CaC2O4(s)  CaO(s) +CO(g)+CO2(g),若前5 min 内生成CaO的质量为11.2 g ,则该段时间内v(CaC204)= mol·min-1;
CaO(s) +CO(g)+CO2(g),若前5 min 内生成CaO的质量为11.2 g ,则该段时间内v(CaC204)= mol·min-1;
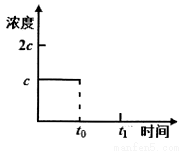
若某时刻达到平衡时c(CO2)= c;t0 时刻,
将容器体积缩小为原来的一半并固定不变,在t1时刻再次达到平衡,
请在右图中画出t0以后此体系中CO2的浓度随时间变化的图像;
II.与化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示)。下表是某温度下几种常见弱酸的电离平衡常数:

回答下列问题:
(4)根据以上条件,请比较同浓度的CH3COONa, NaClO, Na2C03, NaHC03, Na3P04,
NaH2P04, Na2HP04溶液,则它们pH最大的是 (填化学式,下同),pH最小的是
(5)向NaClO溶液中通入过量二氧化碳,发生的离子方程式为
III.(6)取一定量主要含有I-、 Cl一等离子溶液,向其中滴加AgN03溶液,当AgCl开始沉淀时,溶液中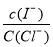 为 。
为 。
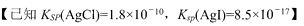
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
根据热化学方程式(101 KPa) S(s) +O2 (g)=SO2 (g); △H=-297.23KJ/mol分析下列说法不正确的是
A.S的燃烧热为297.23KJ/mol
B.S(g) +O2 (g)=SO2 (g) 放出的热量大于297.23KJ
C.S(g) +O2 (g)=SO2 (g) 放出的热量小于297.23KJ
D.形成1molSO2化学键所释放总能量大于断裂1molS(s)和1molO2(g)的化学键所吸收的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com