
IΘΚ≥ΘΈ¬œ¬Θ§ΫΪΡ≥“Μ‘ΣΥαHAΚΆNaOH»ή“ΚΒ»ΧεΜΐΜλΚœΘ§Ζ÷±πΫχ––±ύΚ≈ΈΣΔΌΓΔΔΎΓΔΔέΒΡ Β―ιΘ§ Β―ι ΐΨίΦ«¬Φ»γœ¬±μ
| –ρΚ≈ | HAΈο÷ ΒΡΝΩ≈®Ε»(molΓΛLΘ≠1) | NaOHΈο÷ ΒΡΝΩ≈®Ε»(molΓΛLΘ≠1) | ΜλΚœ»ή“ΚΒΡpH |
| ΔΌ | 0.1 | 0.1 | pHΘΫ9 |
| ΔΎ | c | 0.2 | pHΘΫ7 |
| Δέ | 0.2 | 0.1 | pH<7 |
«κΜΊ¥πΘΚΘ®1Θ©ΗυΨίΔΌΉι Β―ι«ιΩωΘ§Ζ÷ΈωΜλΚœ»ή“ΚΒΡpHΘΫ9ΒΡ‘≠“ρ «_________________ΓΘ
(”ΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)Θ§‘ΎΗΟ»ή“Κ÷–œ¬Ν–ΙΊœΒ Ϋ≤Μ’ΐ»ΖΒΡ «(Χν–ρΚ≈Ή÷ΡΗ)________ΓΘ
AΘ°c(NaΘΪ)ΘΪc(HΘΪ)ΘΫc(OHΘ≠)ΘΪc(AΘ≠) BΘ°c(NaΘΪ)ΘΫc(HA)ΘΪc(AΘ≠)
CΘ°c(HA)ΘΪc(HΘΪ)ΘΫc(OHΘ≠) DΘ°c(NaΘΪ)ΘΪc(HΘΪ)ΘΫc(OHΘ≠)ΘΪc(AΘ≠)ΘΪc(HA)
Θ®2Θ©ΔΎΉι«ιΩω±μΟςΘ§c 0Θ°2molΓΛLΘ≠1(―ΓΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑΘΫΓ±)ΓΘΜλΚœ»ή“Κ÷–άκΉ”≈®Ε»
c(AΘ≠)_____c(NaΘΪ)(―ΓΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑΘΫΓ±)¥”ΔέΉι Β―ιΫαΙϊΖ÷ΈωΘ§ΥΒΟςHAΒΡΒγάκ≥ΧΕ»________NaAΒΡΥ°Ϋβ≥ΧΕ»(―ΓΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑΘΫΓ±)ΓΘ
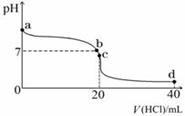 ΔρΘΚ “Έ¬œ¬Θ§»τΫΪ0Θ°1 molΓΛLΘ≠1―ΈΥαΒΈ»κ20 mL 0Θ°1 molΓΛLΘ≠1Α±Υ°÷–Θ§»ή“ΚpHΥφΦ”»κ―ΈΥαΧεΜΐΒΡ±δΜ·«ζœΏ»γœ¬ΆΦΥυ ΨΓΘ Θ®1Θ©NH3ΓΛH2OΒΡΒγάκΖΫ≥Χ Ϋ « ΓΘ
ΔρΘΚ “Έ¬œ¬Θ§»τΫΪ0Θ°1 molΓΛLΘ≠1―ΈΥαΒΈ»κ20 mL 0Θ°1 molΓΛLΘ≠1Α±Υ°÷–Θ§»ή“ΚpHΥφΦ”»κ―ΈΥαΧεΜΐΒΡ±δΜ·«ζœΏ»γœ¬ΆΦΥυ ΨΓΘ Θ®1Θ©NH3ΓΛH2OΒΡΒγάκΖΫ≥Χ Ϋ « ΓΘ
Θ®2Θ©bΒψΥυ Ψ»ή“Κ÷–ΒΡ»ή÷ « ΓΘ
Θ®3Θ©cΒψΥυ Ψ»ή“Κ÷–Θ§άκΉ”≈®Ε»¥”¥σΒΫ–ΓΒΡΙΊœΒΈΣ ΓΘ

| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν– Β―ιΉΑ÷ΟΜρ≤ΌΉςΘ®“―¬‘»Ξ≤ΩΖ÷Φ–≥÷“«ΤςΘ©’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
| ΓΓ | AΘ° |
≈δ÷Ο»ή“Κ | BΘ° |
Β―ι “÷Τ““œ© | CΘ° |
÷Τ±ΗFeΘ®OHΘ©2 | DΘ° |
÷Τ±Η”κ ’Φ·Α±Τχ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΦΉ¥Φ÷ Ή”ΫΜΜΜΡΛ»ΦΝœΒγ≥Ί÷–ΫΪΦΉ¥Φ’τΤχΉΣΜ·ΈΣ«βΤχΒΡΝΫ÷÷Ζ¥”Π‘≠άμ «
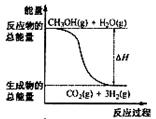
ΔΌCH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΘΜ ΓςH= + 49Θ°0 kJΓΛmolΘ≠1
ΔΎCH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)ΘΜΓςH=Θ≠192Θ°9 kJΓΛmolΘ≠1
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ « Θ® Θ©
AΘ°CH3OHΒΡ»Φ…’»»ΈΣ192Θ°9 kJΓΛmolΘ≠1
BΘ°Ζ¥”ΠΔΌ÷–ΒΡΡήΝΩ±δΜ·»γ”“ΆΦΥυ Ψ
CΘ°CH3OHΉΣ±δ≥…H2ΒΡΙΐ≥Χ“ΜΕ®“ΣΈϋ ’ΡήΝΩ
DΘ°ΗυΨίΔΎΆΤ÷ΣΖ¥”ΠΘΚCH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)ΒΡΓςH>Θ≠192Θ°9kJΓΛmolΘ≠1
 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν–”–ΙΊ Β―ιΒΡΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°÷–ΚΆΒΈΕ® ±Θ§”Ο¥ΐ≤β»ή“Κ»σœ¥ΉΕ–ΈΤΩ
BΘ° Ι”ΟpH ‘÷Ϋ≤βΕ®»ή“ΚpH ±œ»»σ ΣΘ§‘ρ≤βΒΟ»ή“ΚΒΡpH“ΜΕ®ΤΪ–Γ
CΘ°”ΟΦν ΫΒΈΕ®ΙήΝΩ»Γ12.00 mLΗΏΟΧΥαΦΊ»ή“Κ
DΘ°ΒΈΕ®«ΑΒΈΕ®ΙήΡΎΈόΤχ≈ίΘ§÷’ΒψΕΝ ΐ ±”–Τχ≈ίΘ§Υυ≤βΧεΜΐΤΪ–Γ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©
AΘ°≈®Ε»ΨυΈΣ0.1 molΓΛLΘ≠1ΒΡCH3COOH”κCH3COONa»ή“ΚΒ»ΧεΜΐΜλΚœΚσ»ή“Κœ‘Υα–‘Θ§
‘ρΘΚc(CH3COOΘ≠)ΘΦc(CH3COOH)
BΘ°≈®Ε»ΨυΈΣ0.1 molΓΛL-1ΒΡΑ±Υ°”κ―ΈΥαΒ»ΧεΜΐΜλΚœΚσΒΡ»ή“Κ÷–ΘΚc(H+)ΘΫc(OH-) + c(NH3ΓΛH2O)
CΘ°≈®Ε»ΨυΈΣ0.1 molΓΛL-1ΒΡ–ΓΥ’¥ρ»ή“ΚΚΆ«β―θΜ·ΡΤ»ή“ΚΒ»ΧεΜΐΜλΚœΘΚ
c(Na+)+ c(H+)ΘΫ c(CO32-)+ c(OH-) + c(HCO3-)
DΘ°”ΟpHΘΫ3ΒΡHCl»ή“ΚΒΈΕ®10 mL pHΘΫ11ΒΡΑ±Υ°Θ§¥οΒΫΒΈΕ®÷’Βψ”ϻίΈΥαΒΡΧεΜΐ–Γ”Ύ10 mL
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
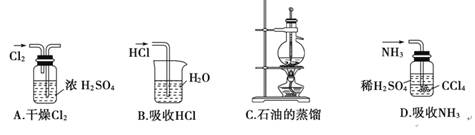
”Οœ¬Ν– Β―ιΉΑ÷ΟΆξ≥…Ε‘”ΠΒΡ Β―ι(≤ΩΖ÷“«Τς“― Γ¬‘)Θ§Ρή¥οΒΫ Β―ιΡΩΒΡΒΡ «(ΓΓΓΓ)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
“―÷ΣX2ΓΔY2ΓΔZ2ΓΔW2ΥΡ÷÷Έο÷ ΒΡ―θΜ·ΡήΝΠ«Ω»θΥ≥–ρΈΣΘΚW2>Z2>X2>Y2Θ§≈–Εœœ¬Ν–―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§ΡήΙΜΖΔ…ζΒΡ «(ΓΓΓΓ)
AΘ°2WΘ≠ΘΪZ2===2ZΘ≠ΘΪW2 BΘ°2XΘ≠ΘΪY2===2YΘ≠ΘΪX2
CΘ°2YΘ≠ΘΪW2===2WΘ≠ΘΪY2 DΘ°2ZΘ≠ΘΪX2===2XΘ≠ΘΪZ2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
Ήι≥…ΚΆΫαΙΙΩ…”Ο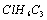
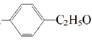 ±μ ΨΒΡ”–ΜζΈο÷–Θ§ΡήΖΔ…ζœϊ»ΞΖ¥”ΠΒΡΙ≤”–Θ® Θ©
±μ ΨΒΡ”–ΜζΈο÷–Θ§ΡήΖΔ…ζœϊ»ΞΖ¥”ΠΒΡΙ≤”–Θ® Θ©
AΘ°10÷÷ BΘ°16÷÷ CΘ°20÷÷ DΘ°25÷÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν–”–ΙΊΨßΧεΒΡ–π ω÷–Θ§’ΐ»ΖΒΡ «Θ® Θ©
AΓΔ ‘ΎSiΨßΧε÷–Θ§Si‘≠Ή””κSi-SiΦϋ÷°±»ΈΣ1:4
BΓΔ‘ΎNaClΨßΧε÷–Θ§ΟΩΗωNa+÷ήΈßΨύάκΉνΫϋΒΡNa+”–6Ηω
CΓΔ‘ΎCsClΨßΧε÷–Θ§”κΟΩΗωCs+ΫτΝΎΒΡCs+”–8Ηω
DΓΔ‘ΎΟφ–ΡΝΔΖΫΕ―ΜΐΒΡΫπ τΨßΧε÷–Θ§ΟΩΗωΫπ τ‘≠Ή”÷ήΈßΫτΝΎΒΡ”–12ΗωΫπ τ‘≠Ή”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com