
科目:高中化学 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:填空题
氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用。
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H= 。(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3 L的恒容密闭容器中,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如下表所示:
温度(K) | 平衡时NH3的物质的量(mol) |
T1 | 2.4 |
T2 | 2.0 |
已知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
①则T1 T2(填“>”、“<”或“=”)。
②在T2 K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)= ,平衡时N2的转化率α(N2)= 。
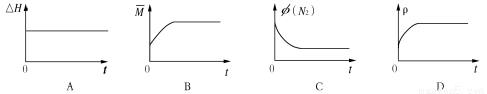
③下列图像分别代表焓变(△H)、混合气体平均相对分子质量( )、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 。
)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 。
(3)某N2H4(肼或联氨)燃料电池(产生稳定、无污染的物质)原理如图1所示。
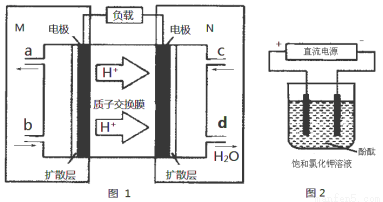
①M区发生的电极反应式为 。
②用上述电池做电源,用图2装置电解饱和氯化钾溶液(电极均为惰性电极),设饱和氯化钾溶液体积为500mL,当溶液的pH值变为13时(在常温下测定) ,若该燃料电池的能量利用率为80%,则需消耗N2H4的质量为 g(假设溶液电解前后体积不变)。
,若该燃料电池的能量利用率为80%,则需消耗N2H4的质量为 g(假设溶液电解前后体积不变)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一6月学业调研化学试卷(解析版) 题型:选择题
下图是产生和收集气体的实验装置示意图,该装置适合于

A.用H2O2溶液和MnO2制取O2
B.用浓盐酸和MnO2制取Cl2
C.用稀硝酸和Cu制取NO
D.用NH4C1和Ca(OH)2制取NH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一6月学业调研化学试卷(解析版) 题型:选择题
一定温度下,恒容容器中发生可逆反应C(s)+ 2H2O(g) CO2(g)+2H2(g),一定能说明该反应已达到平衡状态的是
CO2(g)+2H2(g),一定能说明该反应已达到平衡状态的是
A.生成1molCO2的同时消耗2molH2O
B.n(H2O):n(H2)=1:1
C.2v正(H2O)=v逆(CO2)
D.容器中气体的压强不发生变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一6月学业调研化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 乙烯的结构简式可以表示为CH2CH2
B.甲烷和苯都能发生取代反应
C.乙醇、乙烷和乙酸都可以与钠反应生成氢气
D.石油的分馏和煤的干馏都是物理变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一6月学业调研化学试卷(解析版) 题型:选择题
某元素最高正价氧化物对应的水化物的化学式是HXO4,这种元素的气态氢化物的化学式为
A.HX B.H2X C.XH3 D.XH4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一6月学业调研化学试卷(解析版) 题型:选择题
下列物质分离方法不正确的是
A.用过滤的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.用酒精萃取碘水中的碘
D.用分液的方法分离汽油和氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高二6月学业调研化学试卷(解析版) 题型:选择题
下列实验 结论不正确的是
结论不正确的是
实验操作 | 现象 | 结论 | |
A | 某有机物与溴的四氯化碳溶液混合 | 溶液褪色 | 有机物含碳碳双键 |
B | 乙醇与重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
C | 常温下,将二氧化碳通入苯酚钠溶液 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
D | 苯和苯酚稀溶液分别与浓溴水混合 | 后者产生白色沉淀 | 羟基影响了苯环的活性 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
(1)25℃时,在等体积的 ① pH=0的H2SO4溶液、② 0.05 mol/L的Ba (OH)2溶液、③ pH=10的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比 。
(2)常温下,0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后:
c(CH3COO?) + c(CH3COOH)= mol/L
c(H+) c(CH3COO?) - c(CH3COOH) +2c(OH?) (填“>”、“<”或“=”)
(3)常温下,把pH=11的氢氧化钠溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系是 。
(4)常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,混和液pH=7。则两溶液的体积比是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com