
| A. | 1mol O | B. | 1mol O2 | C. | 1mol氧原子 | D. | 1摩尔小麦 |
分析 摩尔是物质的量的单位,物质的量只能用于描述微观粒子,不能用于宏观物质,如1mol O、1mol O2、1mol氧原子等,不能表示为1摩尔小麦,据此进行判断.
解答 解:A.1molO表示的是1mol氧原子,该表示方法合理,故A正确;
B.1mol O2表示1mol氧气分子,该表示方法合理,故B正确;
C.1mol氧原子,表示1molO,该表示方法合理,故C正确;
D.1mol小麦,物质的量只能描述微观粒子,小麦为宏观物质,不能用摩尔表示,故D错误;
故选D.
点评 本题考查了物质的量的单位-摩尔的应用,题目难度不大,注意物质的量只能用于微观粒子,不能用于宏观物质,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,阳极质量减少6.4g,电路中电子转移的总数为0.2NA | |
| B. | 6.0gSiO2晶体中含有0.2NA个Si-O键 | |
| C. | NA个CH4在标准状况下的体积约为22.4L | |
| D. | 苯与液溴反应生成1mol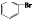 时消耗0.5NA个Br2 时消耗0.5NA个Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
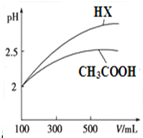 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
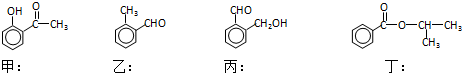
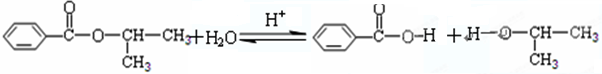 ;
;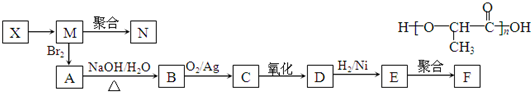
 .
.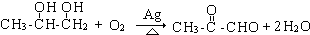 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | B. | 水分子的比例模型: | ||
| C. | 硅的原子结构示意图: | D. | Na2S的电子式 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Br-、CO32- | B. | NH4+、I-、SO32- | C. | Fe2+、I-、SO32- | D. | Fe2+、Br-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
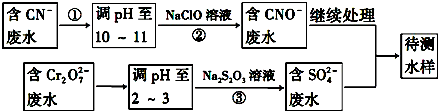
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质的种类很多,它们都能溶解于水 | |
| B. | 蛋白质水解的最终产物是氨基酸 | |
| C. | 蛋白质溶液中加入浓盐酸,颜色变黄 | |
| D. | 蛋白质溶液中加入饱和硫酸铵溶液,蛋白质将变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com