
| 滴定 序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | 6.00 | 31.35 | 25.35 |
分析 (1)盐酸利用酸式滴定管盛放,用标准液盐酸滴定氢氧化钠,选用酚酞作指示剂,溶液开始为红色,滴定终点时变为无色;
(2)由表格数据可知,消耗盐酸为$\frac{25.30mL+25.35mL}{2}$,结合HCl+NaOH=NaCl+H2O、n=cV计算;
(3)结合c(NaOH)=$\frac{c(盐酸)V(盐酸)}{c(NaOH)}$及不当操作对V(盐酸)的影响判断.
解答 解:(1)滴定:用酸式滴定管盛装c mol/L盐酸标准液.实验中选用酚酞作指示剂,当滴入最后一滴盐酸时,溶液由红色变为无色、且半分钟内不变色现象时表示滴定达到终点,
故答案为:酸;滴入最后一滴盐酸时,溶液由红色变为无色、且半分钟内不变色;
(2)由表格数据可知,消耗盐酸为$\frac{25.30mL+25.35mL}{2}$,由HCl+NaOH=NaCl+H2O、n=cV可知,烧碱样品的物质的量浓度的表达式为$\frac{\frac{25.30mL+25.35,mL}{2}×1{0}^{-3}L×cmol/L}{V×1{0}^{-3}L}$,故答案为:$\frac{\frac{25.30mL+25.35,mL}{2}×1{0}^{-3}L×cmol/L}{V×1{0}^{-3}L}$;
(3)a.若滴定前用蒸馏水冲洗锥形瓶,HCl、NaOH的物质的量均不变,则会使测定结果无影响,故答案为:无影响;
b.读数时,若滴定前仰视,滴定后俯视,消耗盐酸偏小,由c(NaOH)=$\frac{c(盐酸)V(盐酸)}{c(NaOH)}$可知,则会使测定结果偏低,故答案为:偏低;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,消耗盐酸偏大,由c(NaOH)=$\frac{c(盐酸)V(盐酸)}{c(NaOH)}$可知,则会使测定结果偏高,故答案为:偏高;
d.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,消耗盐酸偏小,由c(NaOH)=$\frac{c(盐酸)V(盐酸)}{c(NaOH)}$可知,则会使测定结果偏低,故答案为:偏低.
点评 本题考查物质含量的测定实验,为高频考点,把握仪器的使用、中和反应、实验技能为解答关键,侧重分析与实验能力的考查,注意结合反应计算,题目难度不大.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案科目:高中化学 来源: 题型:选择题
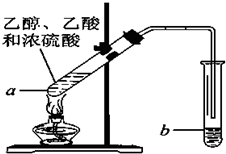
| A. | 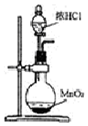 用如图装置制取氯气 | |
| B. | 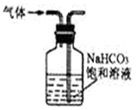 用如图装置除去CO2中的少量SO2气体 | |
| C. | 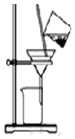 用如图装置分离饱和Na2CO3溶液中的NaHCO3晶体 | |
| D. | 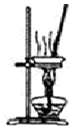 用如图装置将MgCl2.6H2O加热得到MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑦⑧⑨ | B. | ①④⑦⑧⑨⑩ | C. | ①③④⑥⑨⑩ | D. | ①②④⑤⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题. ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
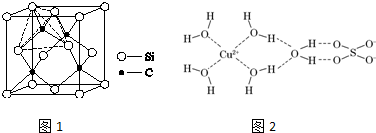
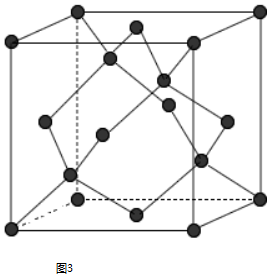
 ;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.
;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
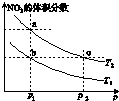 在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )
在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )| A. | a、c两点的反应速率:a>c | B. | 由a点到b点,可以用加热的方法 | ||
| C. | a、c两点气体的颜色:a深,c浅 | D. | a、b两点NO2的转化率:a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
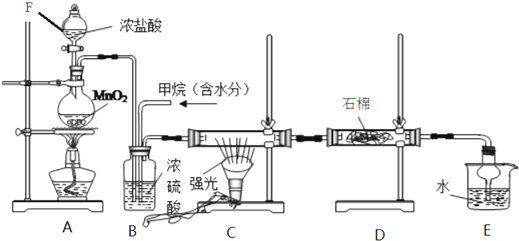
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com