
| A. | 12.6 | B. | 13 | C. | 13.5 | D. | 13.6 |
分析 假设乙烯、乙炔的体积分别为xL、yL,则混合气体消耗氧气为2.8(x+y)L,根据方程式表示出各自消耗氧气的体积,据此列方程计算x、y的比例关系,从而求出混合气体的相对分子量,由此解答.
解答 解:假设乙烯、乙炔的体积分别为xL、yL,则混合气体消耗氧气为2.8(x+y)L,
C2H4+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O
xL 3xL
C2H2+2.5O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+H2O
yL 2.5yL
则3xL+2.5yL=2.8(x+y)L
整理得x=1.5y,所以原混合气体对氢气的相对密度为:$\frac{28x+26y}{\frac{x+y}{2}}$=$\frac{27.2}{2}$=13.6,
故选D.
点评 本题考查混合物计算、烃的燃烧的计算,难度不大,注意利用方程式解答.


科目:高中化学 来源: 题型:选择题
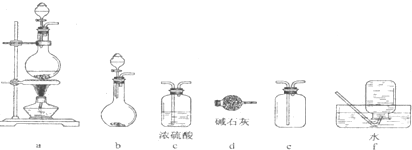
| A. | 加热浓硫酸和乙醇的混合物至170℃制备收集C2H4:连接a→d→f | |
| B. | 制备收集NO2:连接a→c→f | |
| C. | 制备收集Cl2:连接a→d→e | |
| D. | 制备收集NH3:连接b→d→e |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
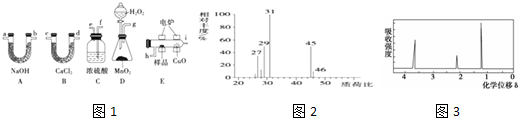
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
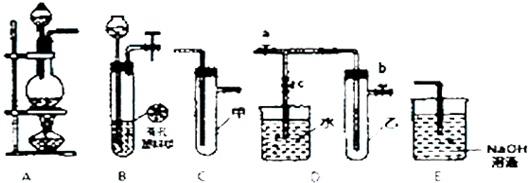
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①②③④⑥ | C. | ①⑤ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
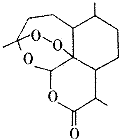 2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )| A. | 2:1 | B. | 3:1 | C. | 12:5 | D. | 16:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,单质铍能与水反应放出H2 | |
| B. | Be(OH)2易溶于水 | |
| C. | Be(OH)2溶于盐酸,也可能溶于NaOH溶液 | |
| D. | BeCl2中各原子中的最外层电子层都满足8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com