
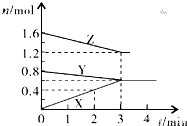
 某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随间变化的曲线如图所示.由图中数据分析
某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随间变化的曲线如图所示.由图中数据分析分析 (1)根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式;
(2)根据化学反应速率v=$\frac{△c}{△t}$进行计算反应开始至2min末X的反应速率;
(3)Z的转化率=$\frac{Z变化的物质的量}{Z初始物质的量}$×100%;根据c(Y)=$\frac{n}{V}$计算出平衡时Y的物质的量浓度.
解答 解:(1)由图象可以看出,反应中Z、Y的物质的量减少,zeZ、Y为反应物,X的物质的量增多,则X应为生成物,
当反应进行到3min时,△n(Y)=0.8mol-0.6mol=0.2mol,△n(Z)=1.6mol-1.2mol=0.4mol,△n(X)=0.6mol,
则△n(Y):△n(Z):△n(X)=1:2:3,参加反应的物质的物质的量之比等于化学计量数之比,则该反应的化学方程式为:Y+2Z?3X,
故答案为:Y+2Z?3X;
(2)反应开始至2min末,X的反应速率为:v(X)=$\frac{\frac{0.6mol}{2L}}{3min}$=0.1mol/(L•min),
故答案为:0.1mol/(L•min);
(3)根据图象可知,平衡时Z的物质的量变化为:△n(Z)=1.6mol-1.2mol=0.4mol,则Z的转化率为:$\frac{0.4mol}{1.6mol}$×100%=25%;
平衡时Y的物质的量为0.6mol,则Y的物质的量浓度为:c(Y)=$\frac{0.6mol}{2L}$=0.3mol/L,
故答案为:25%;0.3mol/L.
点评 本题考查了物质的量随时间变化的曲线,题目难度中等,明确化学反应速率与化学计量数的关系为解答关键,注意掌握反应速率、转化率、物质的浓度的概念及表达式,试题培养了学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
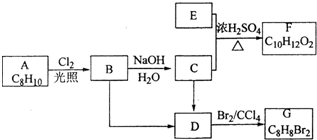 A~G都是有机化合物,它们的转化关系如图:
A~G都是有机化合物,它们的转化关系如图: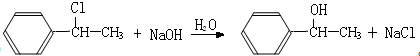 .
. (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | W | Z | 反应体系能量变化 | |
| 甲 | 2mol | 1mol | 放出akJ/mol | ||
| 乙 | 1mol | 1mol | 放出bkJ/mol | ||
| 丙 | 2mol | 2mol | 放出ckJ/mol | ||
| 丁 | 3mol | 2mol | 吸收dkJ/mol |
| A. | c+d<Q | |
| B. | 平衡时,甲、丁容器中X、W的转化率之和大于1 | |
| C. | 平衡时丙容器中Z的物质的量浓度最大 | |
| D. | X的转化率为:甲<乙<丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
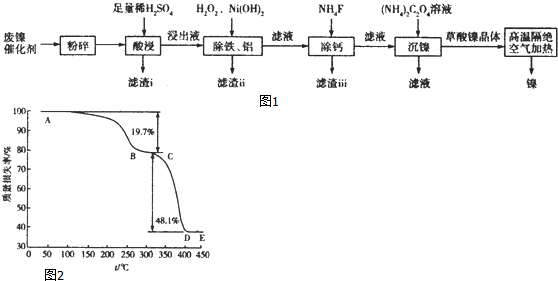
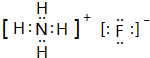
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
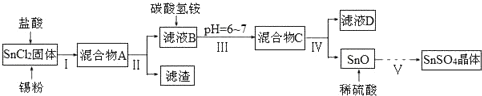
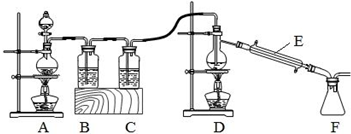
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | s区、d区、ds区都是金属元素 | |
| B. | p区都是主族元素 | |
| C. | 所有族中IIIB中元素种类最多 | |
| D. | 最外层电子数为2的元素都分布在s区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$→_{催化剂、加热}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| B. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCi(aq)}{→}$MgCl2(aq)$\stackrel{△}{→}$ 无水MgCl2 | |
| C. | Al2O3$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$ 固体Al(OH)3 | |
| D. | CH2═CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH$→_{△}^{CuO}$CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com