
已知:
S(s)+O2(g) SO2(g) ΔH=-297.16 kJ·mol-1,
SO2(g) ΔH=-297.16 kJ·mol-1,
2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。
2SO3(g) ΔH=-196.6 kJ·mol-1。
下列说法正确的是 ( )
A.1 mol SO2(g)的能量总和大于1 mol S(s)和1 mol O2(g)的能量总和
B.将2 mol SO2(g)与1 mol O2(g)在一定条件下充分反应,放出196.6 kJ的热量
C.S(g)+O2(g)=SO2(g) ΔH=-Q,Q值小于297.16 kJ
D.当1 mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46 kJ的热量
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源:2014高考化学二轮复习限时集训 专题9电化学原理练习卷A(解析版) 题型:选择题
根据图所示装置,下列说法不正确的是( )
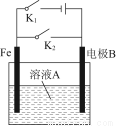
选项开关状态溶液A电极B说明
A打开K1,闭合K2NaCl石墨正极反应:O2+2H2O+4e-=4OH-
B打开K1,闭合K2NaClZn铁制品保护:牺牲阳极的阴极保护法
C打开K2,闭合K1CuSO4Cu铁表面镀铜
D打开K2,闭合K1CuSO4粗铜电解法精炼铜
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题7化学反应速率和化学平衡练习卷A(解析版) 题型:选择题
某研究性活动小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O NH4HCO3+NH3·H2O,经测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是( )
NH4HCO3+NH3·H2O,经测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是( )
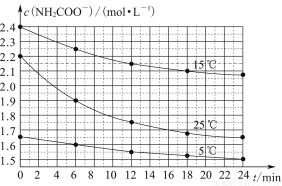
A.0~12 min,初始浓度越大的实验,水解反应速率越大
B.c(NH2COO-)将随反应时间的不断延长而一直减小至0
C.25 ℃时0~6 min,v(NH2COO-)为0. 05 mol·L-1·min-1
D.15 ℃时,第30 min时,c(NH2COO-)为2.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题6物质结构与元素周期律练习卷(解析版) 题型:选择题
下列变化需克服相同类型作用力的是( )
A.碘和干冰的升华 B.硅和C60的熔化
C.氯化氢和氯化钠的溶解 D.溴和汞的汽化
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题5化学反应中的能量变化练习卷(解析版) 题型:选择题
对于反应:C2H4(g)=C2H2(g)+H2(g),2CH4(g)=C2H4(g)+2H2(g),当升高温度时都向右移动。①C(s)+2H2(g)=CH4(g) ΔH1;②2C(s)+H2(g)=C2H2(g)ΔH2;③2C(s)+2H2(g)=C2H4(g) ΔH3。则①②③中ΔH1、ΔH2、ΔH3的大小顺序排列正确的是( )
A.ΔH1>ΔH2>ΔH3 B.ΔH2>ΔH3>ΔH1 C.ΔH2>ΔH1>ΔH3 D.ΔH3>ΔH2>ΔH1
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题4离子反应练习卷(解析版) 题型:选择题
下列事实相对应的离子方程式,不正确的是( )
A.将NaHSO3溶于水,溶液呈弱酸性:HSO3—+H2O SO32—+H3O+
SO32—+H3O+
B.工业上用热的纯碱溶液吸收溴蒸气生成溴酸钠:3Br2+3CO32—=5Br-+BrO3—+3CO2
C.明矾溶液中加Ba(OH)2溶液至SO42—完全沉淀:Al3++2SO42—+2Ba2++3OH-=2BaSO4↓+Al(OH)3↓
D.用惰性电极电解MgCl2溶液产生气体和白色沉淀:Mg2++2Cl-+2H2O Cl2↑+H2↑+Mg(OH)2↓
Cl2↑+H2↑+Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题4离子反应练习卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.氯化钙溶液中通入CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+
B.碳酸钠溶液中逐滴加入等物质的量的盐酸:CO32—+2H+=CO2↑+H2O
C.Ca(ClO)2溶液中通入过量的SO2气体:ClO-+SO2+H2O=HClO+HSO3—
D.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液:Ca2++HCO3—+OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题16物质结构与性质练习卷(解析版) 题型:填空题
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为____________。
②下列叙述不正确的是________。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式________。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是________________________________________________________________________。
②六氰合亚铁离子[Fe(CN)6]4 -中不存在________。
A.共价键 B.非极性键 C.配位键
D.σ键 E.π键
写出一种与 CN-互为等电子体的单质的分子式________。
(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于________区。
(4)一种Al—Fe合金的立体晶胞如图所示。请据此回答下列问题:

①确定该合金的化学式____________。
②若晶体的密度为ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为__________cm。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题13化学实验基础练习卷(解析版) 题型:选择题
下列有关实验操作或方法正确的是( )
A.NaCl溶液蒸发结晶时,蒸发皿中刚好有晶体析出时即停止加热
B.烧碱属于离子化合物,熔点较高,实验室中可选用石英坩埚熔化烧碱
C.滴定时,左手控制滴定管活塞,右手摇动锥形瓶,眼睛注视滴定管中液面的变化
D.用CCl4从碘水中萃取碘,有一步操作为“将分液漏斗倒转过来振荡,使两种液体充分接触”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com