
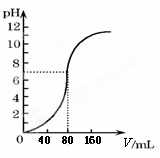
用1.0mol·L-1NaOH溶液中和某浓度硫酸溶液时,其pH
和所加NaOH溶液的体积(V)关系如右图所示。则原硫酸溶
液的物质的量浓度和恰好完全反应后溶液的总体积分别是(设二者混合后体积为二者体积之和)( )
A.0.5mol·L-1 160mL
B.1.0mol·L-1 160mL
C.0.5mol·L-1 80mL
D.1.0mol·L-1 80mL
科目:高中化学 来源: 题型:
下列各项中,含氧原子数不同的是( )
A、质量比为2:1的SO2和O2
B、9g水和23g乙醇(C2H5OH)
C、标准状况下44.8L的一氧化氮和100 ml 5mol/L的硫酸溶液
D、物质的量相同的Na2SO4和FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 == 2Na2CO3 + O2 。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
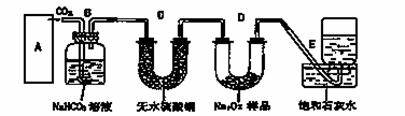
(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图: ;
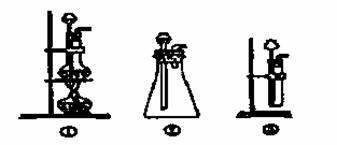
B装置的作用是 ;
C装置内可能出现的现象是 ;
为了检验E中收集到的气体,在取出集气瓶后,用带火星的木条伸入集气瓶内,会出现 。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因: 。(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值 (答大或小),这是由于 。
(5)你认为上述A-E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项: 。(用甲、乙、丙、丁回答)
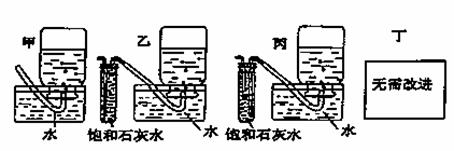
查看答案和解析>>
科目:高中化学 来源: 题型:
对于合成氨工业来说,下列叙述中正确的是( )
A.使用催化剂和施加高压,都能提高反应速率,都对化学平衡状态无影响
B.使用催化剂和施加高压,都能提高反应速率,只有压强对化学平衡状态有影响
C.采用循环操作,能提高NH3的平衡浓度
D.采用循环操作,能加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
I.下列说法不正确的是 (填字母代码)。
A.对于Al(OH)3(s) Al(OH)3(aq)
Al(OH)3(aq) Al3++3OH-,前者为溶解平衡,后者为电离平衡
Al3++3OH-,前者为溶解平衡,后者为电离平衡
B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
C.能源、信息与材料通常被称为现代社会发展的三大支柱
D.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀
E.除去硬水中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2溶解度比
MgCO3的小
II.向含有AgI的饱和溶液中:
(1)加入固体AgNO3,则c(I-) (填“变大”、“变小”或“不变”,下同)。
(2)若改加更多的AgI,则c(Ag+) 。
(3)若改加AgCl固体,则c(I-) ,而c(Ag+) 。
III.用“>”、“<”或“=”填空:
(1)25℃时1mol/L FeCl3溶液的pH 80℃时1mol/L FeCl3溶液的pH。
(2)已知NaHSO3溶液中c(HSO3-)>c(SO32-)>c(H2SO3),则溶液中c(H+) c(OH-)。
(3)常温下,取等物质的量浓度的HA溶液与NaOH溶液等体积混合,测得混合溶液的
pH=8,混合溶液中由水电离出的c(H+)水 NaOH溶液中由水电离出的c(H+)水。
查看答案和解析>>
科目:高中化学 来源: 题型:
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,将得到的红色金属M和金属E进行如下框图所示转化,获得高效净水剂K2EO4.(答题时,化学式及化学方程式中的M、E均用所对应的元素符号表示):
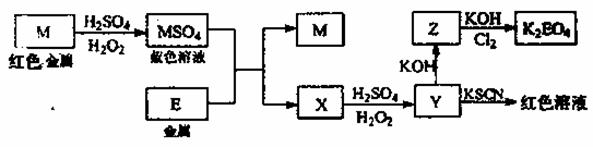
(1)写出M溶于稀H2SO4和H2O2混合液的离子方程式 。
(2)检验X中阳离子的方法和现象是 。
(3)某同学取X的溶液在空气中放置后,酸化并加入KI和淀粉溶液,溶液变为蓝色。试用离子方程式表示溶液变为蓝色的原因: 。
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、烧杯、玻璃棒、漏斗、铁架台外,还需要用到的硅酸盐仪器有 (填写仪器名称)。
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图。A中试剂是盐酸。
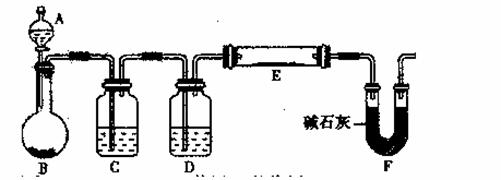
①装置D的作用 ;
②连接好装置并检验装置的气密性后,应首先“加热反应管E”还是“从A瓶中逐滴加入液体”? 在这两步之间还应进行的操作是 。
③该实验设计是否还有不足之处?若有请指出并改进,如没有本问可不答。
(6)试说明K2EO4可用作高效净水剂的原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2S能定量完成下列反应:
R- +H2S(少量) HR + HS-, 2Z-+ H2S(少量)
HR + HS-, 2Z-+ H2S(少量) 2HZ + S2-。
2HZ + S2-。
下列叙述正确的是
A.相同温度下电离平衡常数:Ki1(H2S)>Ki(HZ)>Ki2(H2S)>Ki(HR)
B.结合H+的能力:Z->S 2->R->HS-
C.同温同浓度下,溶液的pH值:NaHS>NaR>Na2S>NaZ
D.HZ与Na2S反应的离子方程式:HZ +S2- HS- + Z-
HS- + Z-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com