
【题目】钠熔融盐燃料电池拥有比锂电池高一倍的能量密度,在同等电池体积下,可让电动汽车行驶距离成倍提升。如图所示是某钠熔融盐燃料电池,其中生成物Y是一种氧化物。下列说法不正确的是
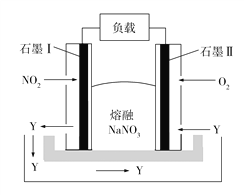
A. 电池工作时,石墨电极Ⅰ上电极反应式为2NO2 2e +O2![]() N2O5
N2O5
B. 电池工作时,![]() 向石墨电极Ⅰ移动
向石墨电极Ⅰ移动
C. 该电池充电时,石墨电极Ⅱ连接电源的负极
D. 电池工作时,外电路中流过1 mol电子,则消耗46 g NO2
 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E、G的原子序数依次增大,在元素周期表中A的原子半径最小(稀有气体元素除外),B与C相邻且C的最外层电子数是次外层的3倍,C、D的最外层电子数之和与G的最外层电子数相等,E是地壳中含量最多的金属元素。回答下列问题:
(1)C在元素周期表中的位置是_________周期、_________族;G的元素符号是_________。
(2)B的原子结构示意图是_________;C与D组成的既含离子键又含共价键的化合物电子式是_________。
(3)E单质能与D的最高价氧化物的水化物浓溶液反应放出氢气,反应的化学方程式是__________________;由上述六种元素中的三种组成的某种盐,水溶液显碱性,将该盐溶液滴入硫酸酸化的KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式是__________________。
(4)由A、B、C、E中的某些元素组成的化合物X、Y、Z、W有如下转化关系:
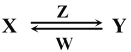
X、Y、Z、W中均由三种元素组成,Z是一种强酸,则Z的化学式是___________,Y溶液与过量W反应的离子方程式是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是( )。
A. 用盐的形式表示:BaSiO3·CuSiO3
B. 用氧化物形式表示:BaO·CuO·2SiO2
C. 易溶于强酸、强碱
D. 性质稳定,不易褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是()
①向溴乙烷中加入硝酸银溶液可检验溴元素
②顺-2-丁烯和反-2-丁烯的加氢产物相同
③苯和溴水混合可制溴苯
④可用银镜反应区分甲酸和乙醛
A.只有①和④B.只有②和③C.只有①和③D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号内的试剂和方法除去下列各物质中的少量杂质,不正确的是( )
A.苯中含有苯酚(浓溴水,过滤)
B.乙醇中的乙酸(CaO固体、蒸馏)
C.乙酸乙酯中含有乙酸(饱和Na2CO3溶液、分液)
D.乙烷中含有乙烯(溴水、洗气)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: __________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有_____________________。
②如何证明晶体已洗净?_______________________。
(4)TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,其目的是:_______________。
(5)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
(6)流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c(Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为__________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.

试回答下列问题:
(1)燃料电池的优点是________;电解质溶液中的OH-移向______极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________.
(4)利用该装置可以处理氮的氧化物和NH3 尾气,总反应为:6NO2 +8NH3=7N2+12H2O,负极反应式为__________。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________;
(2)通过导线的电子数为__________(用NA表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于水玻璃的说法正确的是( )
A. 水玻璃是一种纯净物
B. 水玻璃可作木材防火剂
C. 水玻璃的化学性质稳定,在空气中不易变质
D. 在建筑工业上可以作黏合剂、耐酸水泥掺料,也是用来制造水泥的主要原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金中含有元素:铝、镁、铜、碳,为测定该合金中铝的含量。
Ⅰ 甲同学设计如下实验:
(1)称取样品a g(精确到0.1 g),溶于足量稀盐酸,过滤。
(2)向步骤(1)所得滤液中加入过量的氢氧化钠溶液,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________、____________________________________________。
(3)向步骤(2)所得滤液中通入过量的二氧化碳气体,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________、____________________________________________。
(4)将步骤(3)所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是_________________________________。原样品中铝的质量分数是__________。
Ⅱ 乙同学认为也可以向一定质量的样品中直接加足量氢氧化钠溶液充分反应后,将剩余固体过滤、洗涤、干燥后称量,即可计算该合金中铝的含量。有关反应的离子方程式是____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com