
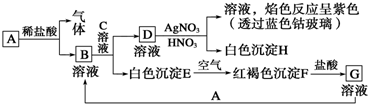
分析 D与硝酸银、硝酸反应得到的溶液,进行焰色反应显紫色,说明D溶液中含有K元素,同时生成白色沉淀H为AgCl,所以D是KCl.白色沉淀E在空气中转化为红褐色沉淀,则E为Fe(OH)2、F为Fe(OH)3,G为FeCl3.B和C反应生成氯化钾和氢氧化亚铁,所以B、C分别是氢氧化钾、氯化亚铁中的一种,G能和A反应生成B,所以A是Fe,B是为FeCl2,C是KOH,Fe与盐酸反应得到氯化亚铁与氢气,据此解答.
解答 解:D与硝酸银、硝酸反应得到的溶液,进行焰色反应显紫色,说明D溶液中含有K元素,同时生成白色沉淀H为AgCl,所以D是KCl.白色沉淀E在空气中转化为红褐色沉淀,则E为Fe(OH)2、F为Fe(OH)3,G为FeCl3.B和C反应生成氯化钾和氢氧化亚铁,所以B、C分别是氢氧化钾、氯化亚铁中的一种,G能和A反应生成B,所以A是Fe,B是为FeCl2,C是KOH,Fe与盐酸反应得到氯化亚铁与氢气.
(1)由上述分析可知,B的化学式为FeCl2,D的化学式为KCl,故答案为:FeCl2;KCl;
(2)KCl溶液与AgNO3溶液反应离子方程式:Ag++Cl-═AgCl↓;
向FeCl3溶液中加入Fe反应离子方程式:2Fe3++Fe═3Fe2+,
故答案为:Ag++Cl-═AgCl↓;2Fe3++Fe═3Fe2+;
(3)Fe与盐酸发生反应:Fe+2HCl=FeCl2+H2↑,生成0.1mol氢气,转移电子数为0.1mol×2×NAmol-1=0.2NA,故答案为:0.2NA.
点评 本题考查无机物推断,是高考中的常见题型,属于中等难度.试题综合性强,难易适中,侧重对学生基础知识的巩固与训练,焰色反应及物质的颜色、特殊反应现象为推断突破口,需要学生熟练掌握元素化合物性质.


科目:高中化学 来源: 题型:解答题
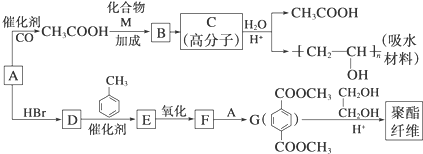
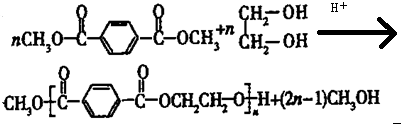 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 沸点不同的液体可用蒸馏的方法分离 | |
| B. | 易溶与难溶的固体混合物可用溶解、过滤、蒸发、结晶的方法分离 | |
| C. | 用酒精可以从碘水中萃取碘 | |
| D. | 汽油和水的化合物不可以用分液漏斗分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200 mL 0.25 mol•L-1 MgCl2溶液 | B. | 200 mL 0.25 mol•L-1 AlCl3溶液 | ||
| C. | 50 mL 1 mol•L-1 NaCl溶液 | D. | 25 mL 0.5 mol•L-1 HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
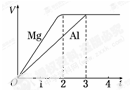 一定质量的镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.下列关于反应的说法错误的是( )
一定质量的镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.下列关于反应的说法错误的是( )| A. | 镁和铝的物质的量之比为3:2 | B. | 镁和铝转移电子数之比为1:3 | ||
| C. | 镁和铝的摩尔质量之比为8:9 | D. | 镁和铝反应所用时间之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若R是硫元素、则C是Na2SO3 | B. | 若R是硅元素、则C是Na2Si03 | ||
| C. | 若R是碳元素、则C是Na2CO3 | D. | 若R是氯元素、则C是NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应2Mg+CO2═2MgO+C△H<0从熵变角度看,可自发进行 | |
| B. | 在密闭容器发生可逆反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-113.0kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,△H变小 | |
| C. | 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2.0×10-12,将等体积的浓度为1.0×10-4mol/L的AgNO3溶液滴入到浓度为1.0×10-4mol/L的KCl和K2CrO4的混合溶液中产生两种不同沉淀,且Ag2CrO4沉淀先产生 | |
| D. | 根据HClO的Ka=3.0×10-8mol/L,H2CO3的Ka1=4.3×10-7mol/L,Ka2=5.6×10-11mol/L,可推测相同状况下,等浓度的NaClO与Na2CO3溶液中,pH前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
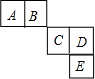 前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子敦之和等于其电子总数的一半,下列说法正确的是( )
前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子敦之和等于其电子总数的一半,下列说法正确的是( )| A. | 元素A、B的所有氢化物中均只含有极性共价键 | |
| B. | 元素C、D形成的简单离子的电子总数不同 | |
| C. | 元素C、D、E形成的常见单质的熔沸点大小:E>D>C | |
| D. | C、D、E三种元素最高价氧化物对应的水化物中D的酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com