
| A. | KClO3 和SO3 溶于水后能导电,故KClO3和SO3为电解质 | |
| B. | 25℃时、用醋酸溶液滴定等浓度NaOH 溶液至pH=7,V醋酸<VNaOH | |
| C. | 向NaAlO2 溶液中滴加NaHCO3 溶液,有沉淀和气体生成 | |
| D. | AgCl 易转化为AgI 沉淀且K(AgX)=c(Ag+ )•c(X-),故K(AgI)<K(AgCl) |
分析 A.电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等.非电解质:在水溶液中或熔融状态下不能导电的化合物;例:有机物,非金属氧化物等;
B.CH3COOH不完全电离,根据电荷守恒可知,c(Na+)+c(H+)=c(OH-)+c(CH3COO-),等体积等浓度混合时显碱性,则中性时应使醋酸过量;
C.NaHCO3溶液与NaAlO2溶液,反应中碳酸氢钠提供氢离子与偏铝酸根反应生成Al(OH)3;
D.AgCl沉淀易转化为AgI沉淀,说明溶解度S(AgCl)>S(AgI),所以K(AgCl)>K (AgI).
解答 解:A.SO3虽溶于水能导电,但导电实质是H2SO4导电,不是三氧化硫导电,三氧化硫属于非电解质,故A错误;
B.醋酸与NaOH溶液反应:CH3COOH+NaOH=CH3COONa+H2O,根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(CH3COO-),若等体积等浓度混合时显碱性,则25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7显中性时应使醋酸过量,即V醋酸>VNaOH,故B错误;
C.氢氧化铝为两性氢氧化物,由于酸性:HCO3->Al(OH)3,根据强酸制备弱酸,NaHCO3溶液与NaAlO2溶液,反应中碳酸氢钠提供氢离子与偏铝酸根反应生成生成Al(OH)3,AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-有沉淀生成,无气体生成,故C错误;
D.向AgCl沉淀中滴入稀KI溶液,会出现白色沉淀AgCl转变为黄色沉淀AgI,说明AgCl沉淀易转化为AgI沉淀,沉淀易转化为更难溶沉淀,越难溶物质其饱和溶液中电离出相应离子浓度越小,故K(AgI)<K(AgCl),故D正确;故选D.
点评 本题考查了电解质、酸碱中和、氢氧化铝、难溶电解质的溶解平衡及沉淀转化等知识,掌握它们的相关本质是解答的关键,题目难度中等.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4+、Fe2+、SO42-、NO3- | B. | Mg2+、K+、Cl-、AlO2- | ||
| C. | Al3+、Na+、SO42-、HS- | D. | Ca2+、H+、NO3-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称量25.20gNaCl | |
| B. | 用250mL的容量瓶配制230mL的碳酸钠溶液 | |
| C. | 用25mL滴定管量取14.80mL的溶液 | |
| D. | 用pH试纸测得溶液的pH为12.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
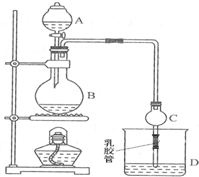 已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3COOCH2CH3+H218O.
CH3COOCH2CH3+H218O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
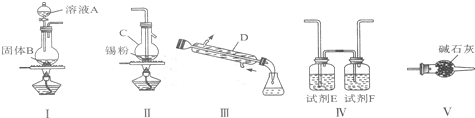
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上常用电解熔融D的氧化物来制备D的单质 | |
| B. | 单质C、D着火,灭火时C不能用泡沫灭火器,但D可以用泡沫灭火器灭火 | |
| C. | 化合物A2B2与C2B2所含化学键类型完全相同 | |
| D. | A、B、C组成的化合物,若溶液浓度为0.01mol/L,则常温下其PH为12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在强碱溶液中:K+、Na+、CO32-、AlO2- | |
| C. | PH=1的溶液中:K+、Cl-、NO3-、Fe2+ | |
| D. | 加入Al能放出H2的溶液中:HCO3-、Na+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸滴在锌粒上:Zn+2H+═Zn2++H2↑ | |
| B. | Ba(OH)2溶液滴入稀硫酸中:Ba2++SO42-═BaSO4↓ | |
| C. | 稀盐酸滴在大理石上:CO32-+2H+═CO2↑+H2O | |
| D. | 氯气通入FeCl2溶液中:Cl2+Fe2+═Fe3++2 Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com