
实验证明,多数能自发进行的反应都是放热反应。对此说法的理解正确的是( )
A.所有的放热反应都是自发进行的
B.所有的自发反应都是放热的
C.焓变是影响反应是否具有自发性的一种重要因素
D.焓变是决定反应是否具有自发性的唯一判据
科目:高中化学 来源: 题型:
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。

填写下面空白:
(1)图中标号处需加入的相应物质分别是
①____________、②____________、③____________、
④____________、⑤____________。
(2)写出①处发生反应的离子方程式________________________________________
________________________________________________________________________;
写出③处发生反应的化学方程式__________________________________________。
(3)铁红的化学式为________;分别写出铁红和氧化铜在工业上的一种主要用途:铁红________________________________________________________________________;
氧化铜________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持及加热仪器已略)。
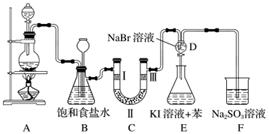
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关反应的化学方程式为__________________________。
装置B中饱和食盐水的作用是____________________。
同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:______________________________________________________________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入的物质为________(填字母)
| 选项 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入少量氯气时,可以看到无色溶液逐淅
变为________色,说明氯的非金属性大于溴。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是______________________________________________。
(4)装置F中用足量的Na2SO3溶液吸收多余氯气,试写出相应反应的离子方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.在饱和氯水中Cl-、NO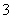 、Na+、SO
、Na+、SO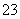 可以大量共存
可以大量共存
B.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应
C.向无色溶液中滴加氯水和CCl4,振荡、静置,下层溶液显紫色说明原溶液中有I-
D.SO2通入碘水中,反应的离子方程式为SO2+I2+H2O===SO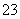 +2I-+2H+
+2I-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验兴趣小组欲采用如图所示的实验装置制备Cl2,同时进行与氯气有关的某些实验,按要求回答问题。
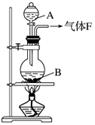
(1)A是浓盐酸,B是二氧化锰,将A滴入B中时发生反应的离子方程式为______________。
(2)甲同学用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2体积在标准状况下小于1.12 L,这是由于反应过程中盐酸浓度变小造成的。请列举导致盐酸浓度变小的原因:__________。
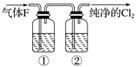
(3)在实验室中,乙同学欲用下图中的装置净化氯气,则瓶①②中应盛放的试剂分别是①__________,②______(填试剂名称)。
(4)丙同学将纯净的Cl2通入一定量石灰乳中来制取漂白粉,若通入224 mL标准状况下Cl2完全反应时,则反应过程中转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有2 mol的SO2的容器中通入过量氧气发生2SO2(g)+O2(g)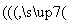 2SO3(g) ΔH=-Q kJ·mol-1(Q>0),充分反应后生成SO3的物质的量______2 mol(填“<”、“>”或“=”,下同),SO2的物质的量______0 mol,转化率______100%,反应放出的热量________ Q kJ。
2SO3(g) ΔH=-Q kJ·mol-1(Q>0),充分反应后生成SO3的物质的量______2 mol(填“<”、“>”或“=”,下同),SO2的物质的量______0 mol,转化率______100%,反应放出的热量________ Q kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于N2(g)+3H2(g)2NH3(g) K1
2NH3(g)N2(g)+3H2(g) K2
试分别写出平衡常数表达式,并判断其关系_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
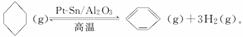 在某温度下,向恒容密闭容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=________。
在某温度下,向恒容密闭容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com