
【题目】下列表示物质的化学式可以称为分子式的是( )
A.SiO2
B.CO2
C.Cu
D.KOH
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】三氧化二锰(Mn2O3)在现代工业上位用广泛,在锂离子电池的制备中有重要的作用。 用软锰矿 (主要成分为MnO2)和硫锰矿(主要成分为MnS)制备高纯度Mn2O3的工艺流程如图所示。

(1) 反应①中会生成一种非金属单质,则该非金属单质是___________,该反应的还原剂是__________。(填化学式)
(2) 操作X为蒸发浓缩、_____________、过滤、洗涤烘干。在洗涤操作中,常用酒精洗涤MnSO4 H2O晶体,主要目的是______________。
(3) Mn2O3与MnO2类似,加热时也能与浓盐酸反应放出Cl2,该反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列7种物质:
①白磷(P4) ②水晶 ③氯化铵 ④氢氧化钙 ⑤氟化钠 ⑥过氧化钠 ⑦干冰
固态时都为晶体,其中既有范德华力,又有非极性键的晶体是 (填写序号,下同),只存在离子键的是 ,熔化时只破坏共价键的是 。
(2)下图是XeF4的结构示意图,据此判断XeF4是 (填“极性”、“非极性”)分子。
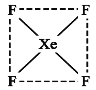
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2 ;②NO2生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A.②③⑥⑦ B.①④⑧ C.只有①④ D.只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月,我国著名药学家屠呦呦因发现治疗疟疾新型药物青蒿素和双氢靑蒿素而获得2015年诺贝尔生理学或医学奖,成为首位获得诺贝尔科学奖的华人女科学家,震惊世界,感动中国。青蒿素(C15H22O5)的结构如图甲所示。请回答下列问题:
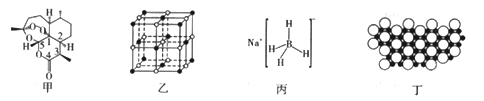
(1)组成靑蒿素的三种元素电负性由大到小的顺序是_________;在基态O原子中,核外存在________对自旋方向相反的电子。
(2)下列关于青蒿素的说法正确的是_______(填序号)。
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均处于同一平面
c.图中数字标识的五个碳原子均只以σ键与其他原子成键
(3)在确定青蒿素结构的过程中,可采用硼氢化钠(NaBH4)作为还原剂,其制备方法为4NaH+ B(OCH3)3![]() NaBH4+3CH3ONa。
NaBH4+3CH3ONa。
①NaH为______晶体,图乙是NaH晶胞结构,则NaH晶体的配位数是______;若晶胞棱长为a,则Na原子间最小核间距为_______。
②B(OCH3)3中B采用的杂化类型是__________。写出一种与B(OCH3)3具有相同空间构型的分子或离子:______________________。
③NaBH4结构如图丙所示,结构中存在的作用力有__________。NaBH4是有机化学中的一种常用还原剂,其在热水中水解生成偏硼酸钠和氢气,该反应的化学方程式为______________。
(4)硼(B)及其化合物在化学中有重要的地位。科学家发现硼化镁在39k时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图丁是该晶体微观空间中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同—平面上。根据图示确定硼化镁的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)写出泡沫灭火器的灭火原理的离子方程式
(2)已知25℃,101 kPa时:
S(s)+O2(g)==SO2(g) H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) H=-53.1 kJ/mol
写出CuS(s)与O2(g)反应生成CuO(s)和SO2(g)的热化学方程式 。
(3)已知常温下AI(OH)3的Ksp=l.0×10-33,若溶液中c(Al3+)为1.0 mol/L,请计算Al3+开始沉淀的pH= 。常温下,浓度均为0.01mol/L的CH3COOH和CH3COONa的混合液中,PH = a,则醋酸的电离常数约为Ka = 。
(4)在常温下,向V L pH=12的Ba(OH)2溶液中逐滴加入一定浓度的NaHSO4稀溶液,当溶液中的Ba2+ 恰好沉淀完全时,溶液pH=11。则Ba(OH)2溶液与NaHSO4溶液的体积比为 ,NaHSO4溶液的物质的量浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.2.4gMg与足量盐酸反应失去0.2NA个电子
B.标准状况下,22.4L水中含有NA个H2O分子
C.1 mol·L-1 Na2CO3溶液中有2NA个Na+
D.78gNa2O2与足量的水反应转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
A.若生成1 mol Fe,则吸收的热量小于a kJ
B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动
C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com