
短周期主族元素A、B、C、D、E的原子序数依次增大,其中只有C是金属元素,B是地壳中含量最多的元素,A元素常见化合价为+1和-1;A与C的最外层电子数相同,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍。下列叙述正确的是
A.元素的原子半径:A<B<C< D< E ( )
B.对应氢化物的热稳定性:D > E
C.B与C、B与D形成的化合物中化学键类型相同
D.五种元素中最高价氧化物对应的水化物酸性最强的是E
【知识点】结构性质位置关系E2
【答案解析】D 解析:短周期主族元素A、B、C、D、E的原子序数依次增大,B是地壳中含量最多的元素,B为氧元素;A元素常见化合价为+1和-1,则A为氢元素;A与C的最外层电子数相同,C是金属元素为Na元素;C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍,则D的核外电子数为3×(1+8)-11=16,则D为硫元素;E的原子序数最大,为主族元素,则E为Cl元素,
A.同周期左到右原子半径减小,电子层越多原子半径越大,则原子半径Na>S>Cl>O,即C>D>E>B,故A错误;
B.非金属性S<Cl,非金属性越强,氢化物越稳定,故对应氢化物的热稳定性:D<E,故B错误;
C.B与C形成Na2O、Na2O2,氧化钠含有离子键,过氧化钠含有离子键、共价键,B与D形成SO3、SO2,只含有共价键,故C错误;
D.非金属性越强,最高价含氧酸的酸性越强,故HClO4的酸性最强,故D正确;故答案选D
【思路点拨】本题考查了结构性质位置关系,推断元素是解题的关键,注意掌握原子半径、氢化物稳定性、最高价含氧酸的酸性比较规律。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
3 mol H2和1 mol N2放入密闭容器中,使用催化剂发生反应:N2(g)+3H2(g)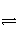
 2NH3(g),从反应开始到平衡过程中,不可能出现的是( )
2NH3(g),从反应开始到平衡过程中,不可能出现的是( )
A.2 mol NH3 B.0.5 mol NH3
C.0.9 mol N2 D.H2和NH3物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
酒精、乙酸和葡萄糖三种溶液,只用一种试剂就能将它们区别开来,该试剂是( )
A.金属钠 B.石蕊试液
C.新制的氢氧化铜悬浊液 D.NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列事实所列出的相应结论正确的是
| 实验事实 | 结论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 结合H+的能力:CO32-<AlO2- |
| D | 常温下白磷可自燃,而氮气须在放电时才与氧 气反应 | 非金属性:P>N |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 B、C、D、E五种短周期元素,元素A最外层电子数与其周期数相等,A与C可形成A2C2和A2C两种化合物,B的最高价氧化物对应的水化物与气体BA3化合生成乙,D+与C2-具有相同的电子数,E元素最高化合价与最低化合价代数和为6。
请回答下列问题:
(1) C在元素周期表中的位置为____________。写出BA3的电子式_______________。
(2)上述元素中,原子半径最大的是____________________(写元素符号)。最高价氧化物对应的水化物中酸性最强的酸是__________________(写化学式)。
(3)化合物乙的水溶液呈酸性,请用离子方程式表示__________________。
(4) A、C、E三种元素按原子个数比1:1:1组成的化合物与BA3反应生成B的单质,写出该反应的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质熔点的排列顺序,不正确的是 ( )。
A.HI>HBr>HCl>HF B.CI4>CBr4>CCl4>CF4
C.NaCl>NaBr>KBr D.金刚石>碳化硅>晶体硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为周期表的一部分,其中的编号代表对应不同的元素。
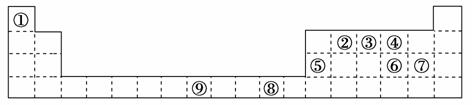
请回答下列问题:
(1)表中属于d区的元素是________(填编号);元素⑧的原子价电子排布式是____________。
(2)③和⑦形成的常见化合物的晶体类型是________;②③④的电负性:________>________>________(用元素符号表示)。判断依据是_________________________________________________________________。
(3)某元素的特征电子排布式(价电子排布式)为nsnnpn+1,该元素为周期表中的________(填编号);该元素与元素①形成的化合物X极易溶于水的原因是__________________________________________________________________
_________________________________________________________________。
(4)②③形成一种超硬、耐磨、耐高温的新型无机非金属材料,则其化学式为________,其熔点比金刚石的________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如右图所示。金刚烷能与卤素发生取代反应,其中一氯一溴金刚烷(C10H14ClBr)的同分异构体数目是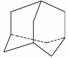 ( )
( )
A.4种 B.6种 C.8种 D.10种
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3(aq)与KSCN(aq)混合时存在下列平衡:
Fe3+(aq)+SCN-(aq)  Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是
A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为
Fe3+(aq)+SCN—(aq)  Fe(SCN)2+(aq) ΔH >0
Fe(SCN)2+(aq) ΔH >0
B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2
C.反应处于D点时,一定有υ正>υ逆
D.A点与B点相比,A点的c(Fe3+)大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com