
| A. | 铜溶于FeCl3溶液中:Cu+2Fe3+=2Fe2++Cu2+ | |
| B. | 石灰石和盐酸反应制CO2:CaCO3+2H+=CO2↑+Ca2++H2O | |
| C. | Ca(ClO)2 溶液中通入过量的SO2:C1O-+SO2+H2O=HClO+HSO${\;}_{3}^{-}$ | |
| D. | 稀Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO${\;}_{3}^{-}$=3Fe3++NO↑+2H2O |
分析 A.反应生成氯化铜、氯化亚铁,遵循电子、电荷守恒;
B.反应生成氯化钙、水、二氧化碳;
C.发生氧化还原反应生成硫酸钙;
D.发生氧化还原反应,遵循电子、电荷守恒.
解答 解:A.铜溶于FeCl3溶液中的离子反应为Cu+2Fe3+=2Fe2++Cu2+,遵循电子、电荷守恒,故A正确;
B.石灰石和盐酸反应制CO2的离子反应为CaCO3+2H+=CO2↑+Ca2++H2O,故B正确;
C.Ca(ClO)2 溶液中通入过量的SO2的离子反应为Ca2++2ClO-+2H2O+2SO2=CaSO4↓+4H++2Cl-+SO42-,故C错误;
D.稀Fe(NO3)2溶液中加入稀盐酸的离子反应为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,故D正确;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
 称为“现代有机合成之父”的伍德沃德曾组织14个国家的110位化学家,协同攻关,探索维生素B12的结构,其结构如图对此结构的下列说法中,正确的是( )
称为“现代有机合成之父”的伍德沃德曾组织14个国家的110位化学家,协同攻关,探索维生素B12的结构,其结构如图对此结构的下列说法中,正确的是( )| A. | 维生素B12属于有机物 | B. | 维生素B12属于无机物 | ||
| C. | 维生素B12属于烃 | D. | 维生素B12属于芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
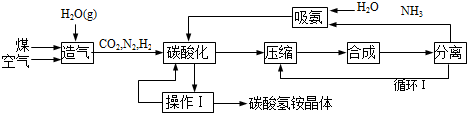

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖水 | B. | 石灰乳 | C. | 氢氧化铁胶体 | D. | 牛奶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液不分层,呈现黄色 | B. | 溶液分层,上层为水层,无色 | ||
| C. | 溶液分层,上层为苯层,紫色 | D. | 溶液分层,下层为苯层,紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,是原电池的装置图,请回答:
如图所示,是原电池的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化物:CaO、Al2O3 | B. | 铵盐:NH3•H2O、NH4Cl | ||
| C. | 酸:H2SO4、NaHSO4 | D. | 碱:NaOH、Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com