
 如图所示,A、B两个装置中两个烧杯分别盛有足量的CuCl2溶液:
如图所示,A、B两个装置中两个烧杯分别盛有足量的CuCl2溶液:分析 (1)把电能转化为化学能的装置是电解池,所以电解池有外接电源;
(2)A为原电池,锌为负极,发生氧化反应,铜为正极,发生还原反应;
(3)B为电解池,阳极发生氧化反应生成氯气,阴极发生还原反应生成铜.
解答 解:(1)A为原电池,B外加电源,应为电解池,故答案为:B;
(2)A为原电池,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为Cu2++2e-=Cu,所以总反应为Cu2++Zn=Cu+Zn2+,
故答案为:负;Zn-2e-=Zn2+;正;Cu2++Zn=Cu+Zn2+;
(3)B为电解池,左边碳棒连接电源负极,为电解池的阴极,发生还原反应,电极方程式为Cu2++2e-=Cu,右边碳棒为阳极,发生氧化反应,电极方程式为2Cl--2e-=Cl2↑,故答案为:阴;Cu2++2e-=Cu;阳;2Cl--2e-=Cl2↑.
点评 本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握原电池和电解池的工作原理,把握电极方程式的书写,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝用于治疗胃酸过多 | |
| B. | 阿司匹林常用于解热镇痛 | |
| C. | 青霉素是一种常用的抗生素 | |
| D. | 非处方药都无毒副作用、可长期大量服用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,分子构型为平面三角形
,分子构型为平面三角形查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正向移动 | B. | 新平衡时,v正(A)=$\frac{p}{m}$v逆(C) | ||
| C. | 气体A的转化率升高 | D. | m+n>p |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO | H2C4H4O6(酒石酸) | H2SO3 |
| 电离平衡常数 | 2.0×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=9.1×10-4 K2=4.3×10-5 | K1=1.3×10-2 K2=6.3×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 六种一溴代物的熔点/°C | 234 | 206 | 213 | 204 | 214 | 205 |
| 对应二甲苯的熔点/°C | 13 | -54 | -27 | -54 | -27 | -54 |
| A. | 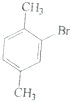 | B. | 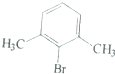 | C. | 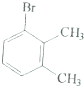 | D. | 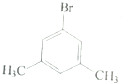 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com