
分析 (1)设原混合物的体积为1L,则反应后气体为0.6L,发生反应3NO2+H2O=2HNO3+NO,利用差量法计算V(NO2),进而计算V(N2),据此解答;
(2)根据c=$\frac{n}{V}$进行计算.
解答 解:(1)设原混合物的体积为1L,反应后气体为0.6L,则:
3NO2+H2O=2HNO3+NO 体积减少
3 1 3-1=2
V(NO2) 1L-0.6L=0.4L
所以,V(NO2)=$\frac{0.4L×3}{2}$=0.6L,则V(N2)=1L-0.6L=0.4L
故:V(N2):V(NO2)=0.4L:0.6L=2:3,答:原混合气体中氮气和二氧化氮气体的体积比2:3;
(2)设原气体体积为VL,而氮气和二氧化氮气体的体积比2:3;所以二氧化氮的体积为:$\frac{3}{5}V$,标况下物质的量为:$\frac{\frac{3}{5}V}{22.4}$mol,则生成硝酸的物质的量为:
$\frac{2}{3}×\frac{\frac{3}{5}V}{22.4}$mol,所以硝酸的物质的量浓度为:$\frac{\frac{\frac{2}{5}V}{22.4}}{\frac{2}{5}V}$=$\frac{1}{22.4}$mol/L,答:硝酸的物质的量浓度为$\frac{1}{22.4}$mol/L.
点评 本题考查混合物的有关计算,难度中等,利用赋值法可以减少计算量,注意差量法的应用.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
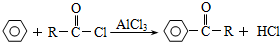
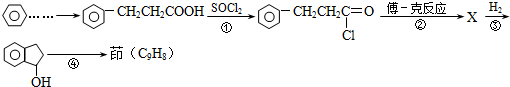
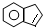 .
.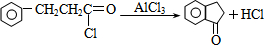 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸亚铁与氢氧化钠溶液混合生成氢氧化亚铁和硫酸钠的反应属于氧化还原反应 | |
| B. | Fe0与一氧化碳反应得到单质铁属于置换反应 | |
| C. | 在自然界中不存在铁单质 | |
| D. | 炽热的铁丝在充满氧气的集气瓶中发生化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
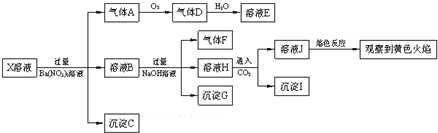
| A. | X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- | |
| B. | 气体F在足量氧气中经催化氧化不可直接生成气体D | |
| C. | 沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 | |
| D. | X中不能确定的离子是Fe2+、SO32-、K+和C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
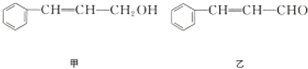
| 分子式 | C14H14O2 |
| 部分性质 | 能使Br2/CCl4褪色 |
| 能在稀H2SO4中水解 |
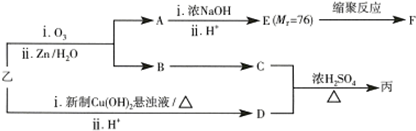
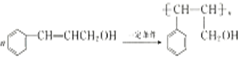 .
.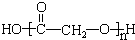 .
.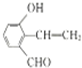 .
.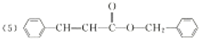 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com