
某研究性学习小组欲测定某绿色粉末Cu2(OH)2CO3·xH2O中的x值,并进行相关实验探究.
已知:Cu2(OH)2CO3·xH2O固体在加热条件下发生反应:
Cu2(OH)2CO3·xH2O![]() 2CuO+CO2↑+(x+1)H2O
2CuO+CO2↑+(x+1)H2O
(Mr[Cu2(OH)2CO3]=222;Mr(CuO)=80;Mr(CO2)=44;Mr(H2O)=18)
[实验一]测定Cu2(OH)2CO3·xH2O中的x值.
(1)准确称取m1g.该粉末样品,置于坩埚中,用酒精灯缓慢加热至完全分解,冷却,称得剩余固体的质量为m2g.加热粉末时,除了坩祸、坩锅钳、三角架、玻璃棒、酒精灯外还要用到的仪器是________,操作中需要用玻璃棒轻轻搅拌固体,目的是________所测得的x值为________(用含m1、m2的代数式表示).
(2)下列是甲、乙两位同学对实验过程中绿色粉末是否已完全分解的判断依据.
甲:观察到粉末变成黑色,不再有水蒸气逸出.
乙:重复加热、冷却、称量,至恒重(两次称量的质量差不超过0.1 g).
你认为其中合理的是________(填“甲”或“乙”).
(3)测定x值还有其它方法.下列是几位同学在实验设计中拟测定的数据,其中无法计算得出x值的是________(填序号).
①只测定生成物CO2、CuO的质量
②只测定生成物CO2、H2O的质量
③只测定反应物Cu2(OH)2CO3·xH2O和生成物CO2的质量
④只测定反应物Cu2(OH)2CO3·xH2O和生成物H2O的质量
[实验二]利用上述反应的分解产物氧化铜氧化乙醇制备乙醛(沸点为20.8℃).
(1)用如图所示装置(图中夹持装置已略去)进行实验时,需要加热的仪器是________(填标号).B装置中收集到的物质有________.
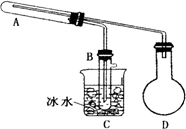
(2)能证明氧化铜氧化乙醇的实验现象是________试管A内发生反应的化学方程式为________.
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 滴定次数 实验数据 |
1 | 2 | 3 | 4 |
| V(醋酸溶液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.00 | 0.200 | 0.10 | 0.00 |
| V(NaOH)/mL(终读数) | 14.98 | 15.20 | 15.12 | 15.95 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
甲醛是世界卫生组织(WHO)确认的致癌物和致畸物质之一。我国规定:室内甲醛(HCHO)含量不得超过0.08mg·m-3。某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你参与并协助他们完成相关学习任务。
原理:KMnO4 ( H+)溶液为强氧化剂,可氧化甲醛。
离子方程式是:4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O 部分装置如下图所示
步骤:(1)配制1.000×10-4mol/L的KMnO4溶液:第一步:用分析天平称取KMnO4固体1.5800g,配成0.01mol/LKMnO4溶液,除了天平、药匙外,需要的玻璃仪器是: 、 、
、 。第二步:用移液管量取上述已配制的溶液 mL,再用上述用到的仪器配制1.000×10-4mol/L的KMnO4溶液。
(2)测定浓度
①用移液管量取8.00mL 1.000×10-4mol·L-1KMnO4溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用。
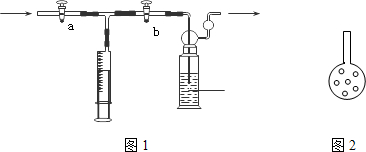
②打开 ,关闭 (填“a”或“b”),用注射器抽取100mL新装修的房屋室内空气。关闭 ,打开 (填“a”或“b”),再推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。重复到第5次注射器推至一半时KMnO4溶液刚好褪色(MnO4-→Mn2+)。
讨论:
(1)计算该居室内空气中甲醛的浓度 mg·m-3,该居室的甲醛 (填是或否)超标。
(2)某同学用该方法测量空气中甲醛的含量时,所测得的数值比实际含量低,探究其可能的原因(假设溶液配制无错误) 。
(3)实验结束后,该小组成员在相互交流的过程中一致认为:实验装置应加以改进:有同学提议,可将插入KMnO4溶液的管子下端改成具有多孔的球泡(右图),有利于提高实验的准确度,其理由是 。
查看答案和解析>>
科目:高中化学 来源:2012届江苏省高二上学期期末考试化学试题(必修) 题型:实验题
甲醛是世界卫生组织(WHO)确认的致癌物和致畸物质之一。我国规定:室内甲醛(HCHO)含量不得超过0.08mg·m-3。某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你参与并协助他们完成相关学习任务。
原理:KMnO4 ( H+)溶液为强氧化剂,可氧化甲醛。
离子方程式是:4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O 部分装置如下图所示
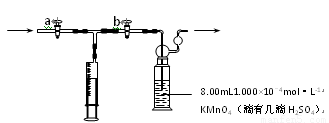
步骤:(1)配制1.000×10-4mol/L的KMnO4溶液:第一步:用分析天平称取KMnO4固体1.5800g,配成0.01mol/LKMnO4溶液,除了天平、药匙外,需要的玻璃仪器是: 、 、
、 。第二步:用移液管量取上述已配制的溶液 mL,再用上述用到的仪器配制1.000×10-4mol/L的KMnO4溶液。
(2)测定浓度
①用移液管量取8.00mL 1.000×10-4mol·L-1 KMnO4溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用。
②打开 ,关闭 (填“a”或“b”),用注射器抽取100mL新装修的房屋室内空气。关闭 ,打开 (填“a”或“b”),再推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。重复到第5次注射器推至一半时KMnO4溶液刚好褪色(MnO4-→Mn2+)。
讨论:
(1)计算该居室内空气中甲醛的浓度 mg·m-3,该居室的甲醛 (填是或否)超标。
(2)某同学用该方法测量空气中甲醛的含量时,所测得的数值比实际含量低,探究其可能的原因(假设溶液配制无错误) 。
(3)实验结束后,该小组成员在相互交流的过程中一致认为:实验装置应加以改进:有同学提议,可将插入KMnO4溶液的管子下端改成具有多孔的球泡(右图),有利于提高实验的准确度,其理由是 。

查看答案和解析>>
科目:高中化学 来源:2010年高三备考“好题速递”系列(20) 题型:实验题
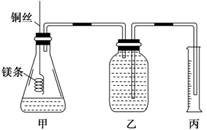 |
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol·L-1的盐酸溶液;
②用 (填仪器名称并注明规格)量取10.0 mL 1.0 mol·L-1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少
为 ;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL
请将上述步骤补充完整并回答下列问题。
(1)用文字表述实验步骤④中检查装置气密性的方法: 。
(2)实验步骤⑤中应选用 (填序号)的量筒。
A.100 mL B.200 mL C.500 mL
读数时除恢复到室温外,还要注意 。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm= ,若未除去镁条表面的氧化膜,则测量结果 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com