
足量的锌与酸反应,欲使制取氢气的反应速率尽可能大,选用的反应条件正确的组合是
①锌粒 ②锌粉 ③加少量的硫酸银的饱和溶液 ④1mol/L的盐酸 ⑤5mol/L的硝酸
⑥1mol/L的硫酸 ⑦加热 ⑧加大量的硫酸铜晶体 ⑨不断振荡 ⑩加大体系的压强
A.②③⑥⑦⑨ B.①③⑤⑦⑩ C.②④⑥⑦⑧⑨ D.②⑦⑧⑨⑩
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
在周期表中相邻的短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。W原子的最外层电子数比Y多2个。下列叙述正确的是
A.Y的最高价氧化物可与氢氧化钠溶液反应
B.最高价氧化物的水化物酸性 Z>X
C.气态氢化物的稳定性 Z>W
D.原子半径 Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学实验小组通过系列实验探究钠及其化合物的性质,下列实验操作及现象与预期 实验目的或实验结论不一致的是
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 原溶液中有Na+无K+ |
| B | 在0.1 mol/L的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 | 验证盐类水解反应是吸热反应 |
| C | 用镊子从煤油中取出金属钠,切下绿豆大小的钠块,用滤纸吸干钠块表面的煤油,小心放入装有苯和水的试管中,钠块在苯与水界面上下浮动 | 比较钠、水和苯三种物质的密度大小 |
| D | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | NaHCO3的溶解度比Na2CO3的小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,不能说明反应
A(s)+2B(g)  C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述中不符合生产实际的是
A:电解熔融Al2O3制金属铝,用铁作阳极
B:电解法精炼粗铜,用纯铜作阴极
C:电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D:在镀件上镀锌,用锌用阳极,硫酸锌作电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央滴入浓硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)当杠杆为绝缘体时,A端比B端 (填高、低、不变。下同);当杠杆为导体时,A端比B端 。
(2)依据氧化还原反应:Fe+Cu2+=Fe2++Cu设计的原电池如下图所示,其中Y为可溶性硫酸盐。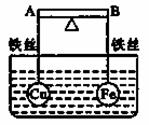
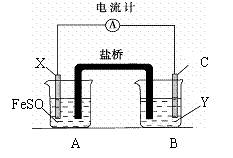

请回答下列问题:
①电解质溶液Y是 ;(填化学式)
②X电极发生的电极反应为 ;
③装置中盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是________。
A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
C.盐桥中的K+、Cl-都向左侧烧杯移动
D.盐桥中的K+、Cl-几乎都不移动
(3)把(2)中盐桥改为铁棒插入A、B池中,其它不变,电流计的指针 (填“会”、“不会”)发生偏转,A装置名称 填(“原电池”或“电解池”),A中溶液浓度 (填增大、不变、变小),铜棒的电极名称为 (填“正极”、“负极”、“阴极”或“阳极”)
(4)把(2)中盐桥改为铜棒,其它不变,电流计的指针 (填“会”、“不会”)发生偏转,理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知
| W | X | |
| Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Z
B.Z和Y元素的氧化物对应水化物的酸性Z一定强于Y
C.简单阴离子的还原性:X<Y
D.最简单氢化物的沸点:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
A.强酸溶液产生较多的氢气
B.两者产生等量的氢气
C.无法比较两者产生氢气的量
D.弱酸溶液产生较多的氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com