
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),生成物并不改变的是
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.NaAlO2和HCl
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
下面提到的问题中,与盐的水解有关的是
①明矾和FeCl3可作净水剂 ②为保存FeCl3溶液,要在溶液中加少量盐酸
③实验室配制AlCl3溶液时,应先把它溶在盐酸中,而后加水稀释
④NH4Cl与ZnCl2溶液可作焊接中的除锈剂
⑤实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞;
⑥用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂;⑦在NH4Cl或AlCl3溶液中加入金属镁会产生氢气
⑧长期使用硫酸铵,土壤酸性增强;草木灰与铵态氮肥不能混合施用
⑨比较NH4Cl和Na2S等溶液中离子浓度的大小或某些盐溶液的酸碱性
A.①④⑦ B.②⑤⑧ C.③⑥⑨ D.全部
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
根据相关化学原理,下列判断正确的是
A.若X是原子晶体,Y是分子晶体,则熔点:X<Y
B.若KXO3+Y2===2KYO3+X2,则氧化性:Y2> X2
C.若R2— 和M+的电子层结构相同,则原子序数:R>M
D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:填空题
(13分)氧化还原反应在工农业生产和日常生活中有广泛运用。
(1)罐头厂在装食物罐头时通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类防腐剂应具有 。 (填“氧化性”或“还原性”);
(2)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 。(填“氧化作用”或“还原作用”);
(3)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。
(4)在下列的空白处填写最适宜的除杂试剂,并写出相应的离子方程式
① FeCl2中含少量FeCl3杂质 , 。
② FeCl3中含少量FeCl2杂质 , 。
③ FeSO4中含少量CuSO4 杂质 , 。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:选择题
氧化还原反应的实质和相应的规律是
A.化合价的升降,化合价的升高和降低的总数相等
B.电子的转移,得电子总数和失电子总数相等
C.得氧和失氧,氧原子数目不变
D.物质的种类发生改变,质量守恒定律
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列关于氯气或氯水的叙述不正确的是
A.氯气能使润湿的淀粉碘化钾试纸变蓝
B.新制的氯水呈黄绿色是因为在溶液中溶有氯气分子
C.与久置氯水不同,在新制氯水中加入硝酸银溶液后无白色沉淀
D.氯水久置后,会使溶液酸性增强
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二上学期第三次月考化学试卷(解析版) 题型:选择题
在FeCl3溶液中滴加无色的KSCN溶液后,有以下可逆反应存在:FeCl3+3KSCN  Fe(SCN)3 +3KCl。已知Fe(SCN)3呈红色,则在该平衡体系中加入少量KCl晶体后(忽略溶液体积的变化),红色将
Fe(SCN)3 +3KCl。已知Fe(SCN)3呈红色,则在该平衡体系中加入少量KCl晶体后(忽略溶液体积的变化),红色将
A.变深 B.变浅 C.不变 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省乐山市高三第一次调查研究考试理综化学试卷(解析版) 题型:填空题
(12分)
A、B、C是短周期非金属元素,核电荷数依次增大。A原子外围电子排布为ns2np2,C是地壳中含量最多的元素。D、E是第四周期元素,其中D原子核外未成对电子数在同周期中最多。E原子最外层只有1个电子,其余各层均排满。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)分子(AB)2中键与键之间的夹角为180°,并有对称性,每个原子最外层电子数均满足八电子,其结构式为 ,1mol该分子中含有 键的物质的量为 。
键的物质的量为 。
(3)基态D原子的外围电子排布式为 。DO2Cl2熔点:-96.5℃,沸点:117℃,则固态DO2Cl2属于 晶体。
(4)E的氢化物的晶胞结构如图所示
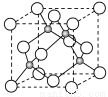
其化学式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com