
【题目】化学反应A2(g) + B2(g)=2AB(g) 的能量变化如图所示,下列叙述中正确的是( )
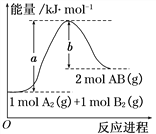
A. 每生成2mol AB(g) 共吸收b kJ热量
B. 该反应热ΔH = +(a-b) kJ·mol-1
C. 反应物的总能量大于生成物的总能量
D. 断裂1 mol A—A键,放出a kJ能量
科目:高中化学 来源: 题型:
【题目】关于SO2的叙述中正确的是( )
A.它可使石蕊试液褪色
B.通入BaCl2溶液中,生成白色沉淀
C.SO2通入氢氧化钠与酚酞的混合溶液中红色变浅直至褪去
D.等物质的量的Cl2和SO2通入品红溶液中,品红溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)实验室中常用NaOH溶液来进行洗气和提纯,当用100 mL 3 mol/L的NaOH溶液吸收标准状况下4.48 L CO2时,所得溶液中各离子浓度由大到小的顺序为________。
(2)常温下向一定体积的0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是________(填字母,下同)。
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中![]() 不变
不变
D.当溶液极稀时,溶液中![]() 减小
减小
(3)①常温下,将V1 mL 0.15 mol/L稀硫酸与V2 mL 0.1 mol/L NaOH溶液混合,所得溶液的pH为1,则V1∶V2=________(溶液体积变化忽略不计)。
②常温下,将V1 mL pH=3的HA溶液与V2 mL pH=11的NaOH溶液混合,则下列说法正确的是________。
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(4)常温下,几种离子开始沉淀时的pH如表所示:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液时,________(填离子符号)先沉淀,Ksp[Fe(OH)2]________Ksp[Mg(OH)2](填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面列出了几组物质,请将正确的序号填写在空格上。
①金刚石与“足球烯”C60; ②HCHO和CH3CHO; ③CH3CH2OH和CH3OCH3;④CH4和CH3CH2CH3;⑤D与T ; ⑥CH2=CH—CH2—CH3和CH3—CH=CH—CH3;⑦氧气(O2)与臭氧(O3)
同位素_________________;同系物_____________ ;
同素异形体_____________;同分异构体______________。
(2)现有下列六种有机物a.乙烷 b.乙烯 c.苯 d.乙醇 e.乙酸 f.CH2===CH—COOH g.CH2OH(CHOH)4CHO h.乙酸乙酯
①能与Na和NaOH溶液都反应的是_____________。
②分子内所有原子一定在同一平面上的有___________。
③常温下可能与溴水发生加成反应的有_____________。
④在一定条件下能发生酯化反应的有_______________。
⑤能与新制Cu(OH)2悬浊液反应的有________________。
⑥能发生水解反应的有______________。
(3)现有 A:CH3CH2OH; B:CH2OH—CH2OH;
C:CH2OH—CH(OH)—CH2OH三种有机物:
①等物质的量的这三种有机物完全燃烧耗氧量之比为______________;
②写出A与金属钠反应的化学方程式:_____________________________。
③等物质的量的这三种有机物与足量金属钠反应,同温同压下产生氢气的体积比为:__________________________。
④写出B在铜作催化剂的条件下与氧气反应的方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶质分子(或离子)和水分子结合后成水合分子(水合离子)的过程是( )
A.物理过程,吸收热量
B.化学过程,吸收热量
C.物理过程,放出热量
D.化学过程,放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每到冬天就会出现大雾天气,能见度不到10米,致使汽车行驶受阻,下列关于雾的说法正确的是( )
A.无法确定雾中水滴的直径大小 B.不会产生丁达尔现象
C.雾中水滴的直径在1nm~100nm间 D.雾中水滴的直径小于1nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是( )
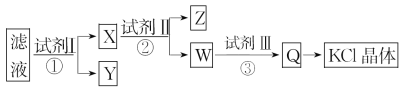
A.起始滤液的pH=7
B.试剂Ⅰ为Ba(NO3)2溶液
C.步骤②中加入试剂Ⅱ的目的是除去B![]()
D.图示的步骤中必须要经过2次过滤操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料,某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下实验方案。
(1)实验原理。
AlN溶于浓的强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程_________。
(2)实验装置。

如图C装置中球形干燥管的作用是_________________________。
(3)实验过程。
①连接好实验装置________,然后称得C装置的质量为yg。
②称取xg AlN样品置于A装置中;塞好胶塞,关闭________打开________(填“K1”或“K2”);通过分液漏斗加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,称得C装置的质量变为zg,通入氮气的目的是__________________,装置B的作用是__________________________。
(4)数据分析。
①AlN的质量分数为________。(相对原子质量Al:27,N:14)
②由于装置存在缺陷,导致测定结果偏高,请提出改进意见________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com