
| m |
| M |
| V |
| Vm |
| N |
| NA |
| 1 |
| 2 |
| 1 |
| 2 |
| 12.4g |
| 0.2mol |
| b |
| a |
| b |
| a |
| 21.6g |
| 0.2mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| W | ���ڱ���ԭ�Ӱ뾶��С��Ԫ�� |
| U | �ؿ��к������Ľ���Ԫ�� |
| R | ����ռ���������1/5 |
| T | M������6������ |
| X | �����������Ǵ�����������2�� |
| Y | �⻯��ˮ��Һ�ʼ��� |
| Z | Ԫ�����������+7�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��23g�����Ʊ�Ϊ������ʱ�õ��ĵ�����ΪNA |
| B����״���£�18gˮ�����ĵ�����ĿΪ18NA |
| C����״���£�22.4 L����������ԭ����ĿΪ2NA |
| D�����³�ѹ�£�2.8g N2��CO�Ļ����������ԭ����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 mol CH4 ��������O2��Ħ����������32 g |
| B��1 mol�κ������ж�������ͬ��ԭ���� |
| C��0.5 mol NaClԼ����6.02��1023������ |
| D��1 mol?L-1 KCl��Һ�к�������1 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ��42g ��ϩ�Ͷ�ϩ��������У����Լ���Ϊ6NA |
| B��100 mL 0.1 mol?L-1 Na2CO3��Һ�У�����������0.03NA |
| C����״���£�11.2L��O2��NO�Ļ���ﺬ�еķ�����ԼΪ0.5��6.02��1023 |
| D��6.4g SO2������������Ӧ����SO3��ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����� | Ԥ����������� |
| ���� ���ۣ� | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
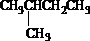
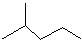
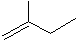
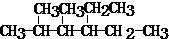
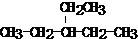
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com