
| A | B | C | D | |
| 正极 | Zn | Zn | 碳棒 | Cu |
| 负极 | 碳棒 | Fe | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | CuSO4 | ZnCl2 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、Q1+Q2<2Q3 |
| B、Q1+Q2>2Q3 |
| C、Q1+Q2<Q3 |
| D、Q1+Q2>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、氨甲环酸、氨甲苯酸都既能溶于盐酸,又能溶于NaOH溶液 |
| B、氨甲环酸、氨甲苯酸都能发生取代、氧化、缩聚等反应 |
| C、氨甲环酸、氨甲苯酸中各有5种不同的氢原子 |
| D、氨甲苯酸和苯丙氨酸互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌锰干电池工作一段时间后碳棒变细 |
| B、氢氧燃料电池可将热能直接转化为电能,是环境友好型电池 |
| C、铅蓄电池是一次电池,对环境有污染 |
| D、乙醇不能做锂电池内部的电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(SO42-)>c(HSO3-)>c(SO32-)>c(H2SO3) |
| B、c(K+)>c(SO32-)>c(SO42-)>c(HSO3-)>c(H+)>c(OH-) |
| C、c(K+)═c(HSO3-)+2c(SO32-)+2c(SO42-) |
| D、c(K+)+c(H+)═c(HSO3-)+c(SO32-)+c(SO42-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
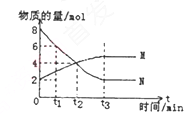
| A、t3时,反应达到最大限度 |
| B、t2,正、逆反应速率相等,达到平衡 |
| C、反应的化学方程式:N?2M |
| D、t1时N的浓度是M浓度的4倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com