
一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4·H2O)是一种重要的染料及农药中间体。请回答下列相关问题:
(1)Cu的核外电子排布式为 。
(2)N的L层中有 对成对电子;N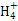 立体构型是 ,其中心原子的杂化方式为 。
立体构型是 ,其中心原子的杂化方式为 。
(3)氨水溶液中存在多种氢键,任表示出其中两种 ;
(4)[Cu(NH3)4]SO4·H2O中呈深蓝色的离子是 ,该微粒中的“电子对给予一接受键”属于 键;
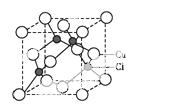
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式 。
科目:高中化学 来源: 题型:
化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言。下列化学用语中,书写错误的是( )
A.硫离子的结构示意图: B.NH4Cl的电子式:
B.NH4Cl的电子式:
C.CO2的电子式:  ············ D.次氯酸的结构式:
············ D.次氯酸的结构式:
查看答案和解析>>
科目:高中化学 来源: 题型:
磷矿石主要以磷酸钙〔Ca3(PO4)2·H2O〕和磷灰石〔Ca5(OH)(PO4)3〕等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。
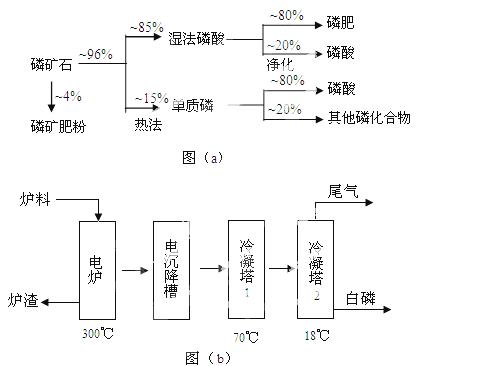
部分物质的相关性质如下:
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水,具有还原性 |
| SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 ℅。
(2)以磷灰石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:  。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品
。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品 磷酸 吨。
磷酸 吨。
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是: (填化学式)冷凝塔1的主要沉积物是: 冷凝塔2的主要沉积物是:
(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾 气先通入纯碱溶液,
气先通入纯碱溶液, 可除去
可除去 
再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是:  。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有几组物质的熔点( ℃)数据:
| A组 | B组 | C组 | D组 |
| 金刚石:3 550 ℃ | Li:181 ℃ | HF:-83 ℃ | NaCl:801 ℃ |
| 硅晶体:1 410 ℃ | Na:98 ℃ | HCl:-115 ℃ | KCl:776 ℃ |
| 硼晶体:2 300 ℃ | K:64 ℃ | HBr:-89 ℃ | RbCl:718 ℃ |
| 二氧化硅:1 723 ℃ | Rb:39 ℃ | HI:-51 ℃ | CsCl:645 ℃ |
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是____________________。
(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于_________________。
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同, b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图为 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中 既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥结构的酸是 。(填化学式)
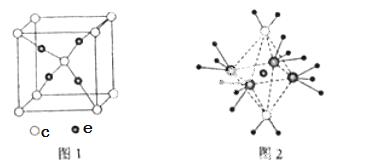
(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 。
(5)这5种元素形成 的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是
的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是  ,判断理由是 。
,判断理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:_____________________,
其中含有的化学键是______________,属于晶体类型为________。
(2)用电子式表示Y2O的形成过程______________________。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是________(填化学式)。
(4)XH3、H2Z和HW三种化合物,其空间构型分别为________、________、________。其中一种与另外两种都能反应的是______________(填化学式),其生成物晶体类型分别属于________、________。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
碳、氢、氟、氮、硅等非金属元素与人类的生产 生活息息相关。回答下列问题。
生活息息相关。回答下列问题。
(1)写出硅原子的电子排布式________。C、Si、N的电负性由大到小的顺序是________。
(2)氟化氢水溶液中存在的氢键有________种。
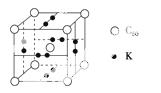
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为________。
(4)继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点Si60>N60>C60,而破坏分子所需要的能量N60>C60>Si60,其原因是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
A.若M(甲)<M(乙),则气体的压强:甲>乙
B.若M(甲)>M(乙),则气体的摩尔体积:甲<乙
C.若M(甲)>M(乙),则气体体积:甲<乙
D.若M(甲)<M(乙),则分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3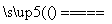 2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com