
| A、n=m+17Vc | ||||
B、c=
| ||||
C、p=m+
| ||||
D、
|
| V |
| Vm |
| n |
| V |
| ||
| ||
| 17Vc |
| 1000 |
| bL |
| 22.4L/mol |
| 1000b |
| 11.2V |
| ||
| ||
| 1 |
| 2 |
| cV |
| 125 |
| m |
| 24 |
| 5m |
| 3 |
| m |
| 27 |
| 1 |
| 2 |
| 17m |
| 9 |
| 5m |
| 3 |
| 17m |
| 9 |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
| A、石蕊层仍为紫色,有机层无色 |
| B、石蕊层为三层环,由上而下是红、紫、红 |
| C、石蕊层有两层,上层为紫色,下层为蓝色 |
| D、石蕊层为三层环,由上而下是蓝、紫、红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
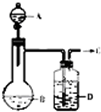 为了制取干燥纯净的气体C,可用如下图所示装置.生成C的速度可通过调节滴入液体A的速度的方法来控制,已知C是一种无色无味、不能使酸碱指示剂变色,也不会在空气中燃烧的气体.
为了制取干燥纯净的气体C,可用如下图所示装置.生成C的速度可通过调节滴入液体A的速度的方法来控制,已知C是一种无色无味、不能使酸碱指示剂变色,也不会在空气中燃烧的气体.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在配制牛肉膏蛋白胨固体培养基时,需加入琼脂,不需要添加NaCl |
| B、利用DNA在不同浓度的NaCl溶液中的溶解度不同,粗提取DNA |
| C、在腐乳制作过程中,装瓶时需逐层等量加入NaCl,以防杂菌污染 |
| D、将哺乳动物的成熟红细胞浸泡于0.9%的NaCl溶液中,用以制备纯净的细胞膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
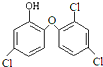
| A、三氯生的分子式是C12H7Cl3O2 |
| B、三氯甲烷与甲烷均无同分异构体 |
| C、1 mol三氯生最多能与6 mol H2反应 |
| D、1 mol三氯生最多能与4mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤加强热而分解的过程叫做煤的干馏 |
| B、煤干馏的目的是得到冶金用的优质焦炭 |
| C、煤的干馏和石油的分馏的本质差别是:干馏是物理变化,而分馏是化学变化 |
| D、工业上苯等芳香烃原料可由煤干馏得到,其存在于干馏所得的焦炉气中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
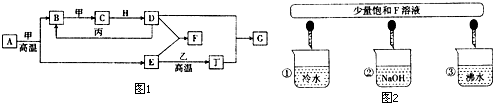
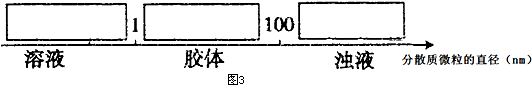
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B、根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3 |
| C、在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化 |
| D、可以推理得到Cl2+FeBr2═FeCl2+Br2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com