
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为________。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是________(填序号)。
a.Cl2、Br2、I2的熔点
b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性
d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液 NaClO3溶液
NaClO3溶液 KClO3晶体①完成Ⅰ中反应的总化学方程式:
KClO3晶体①完成Ⅰ中反应的总化学方程式:
 NaCl+
NaCl+ H2O===
H2O=== NaClO3+
NaClO3+ ________。
________。
②Ⅱ中转化的基本反应类型是________________,该反应过程能析出KClO3晶体而无其他晶体析出的原因是____________________________________。
(4)一定条件下,在水溶液中1 mol Cl-、ClO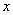 (x=1,2,3,4)的能量(kJ)相对大小如右图所示。
(x=1,2,3,4)的能量(kJ)相对大小如右图所示。
①D是________(填离子符号)。
②B→A+C反应的热化学方程式为________________(用离子符号表示)。

(1) (2)b、c (3)①
(2)b、c (3)① NaCl+
NaCl+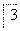 H2O===
H2O=== NaClO3+
NaClO3+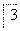 H2↑
H2↑
②复分解反应
室温下,氯酸钾在水中的溶解度明显小于其他晶体
(4)①ClO ②3ClO-(aq)===ClO
②3ClO-(aq)===ClO (aq)+2Cl-(aq) ΔH=-117 kJ·mol-1
(aq)+2Cl-(aq) ΔH=-117 kJ·mol-1
[解析] (1)与氯元素同族的短周期元素为F,F的原子结构示意图为 。
。
(2)Cl2、Br2、I2都是分子晶体,其熔点受分子间作用力影响,与非金属性无关,a项错误;单质的氧化性越强则其元素的非金属性越强,b项正确;非金属性强弱可用气态氢化物的稳定性判断,c项正确;卤素氢化物的酸性可用来判断氢原子与卤素原子形成的共价键强弱,d项错误。(3)①根据氧化还原反应的化合价升降法配平可得:NaCl+3H2O===NaClO3+3H2↑;②步骤Ⅱ发生的反应NaClO3+KCl===KClO3↓+NaCl↑,各元素的化合价没有变化,则该反应属于复分解反应。在室温下,氯酸钾在水中的溶解度小于其他晶体,则有氯酸钾晶体析出而无其他晶体析出。(4)①从图可知D中氯元素的化合价为+7,则D为ClO ;②从图中可知:A为Cl-,B为ClO-,C为ClO
;②从图中可知:A为Cl-,B为ClO-,C为ClO , B→A+C的氧化还原反应用升降法配平可得该热化学方程式为3ClO-(aq)=== ClO
, B→A+C的氧化还原反应用升降法配平可得该热化学方程式为3ClO-(aq)=== ClO (aq)+ 2Cl-(aq) ΔH=(63 kJ/mol+2×0)-3×60 kJ/mol=-117 kJ/mol。
(aq)+ 2Cl-(aq) ΔH=(63 kJ/mol+2×0)-3×60 kJ/mol=-117 kJ/mol。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
关于如图所示装置的叙述,正确的是( )
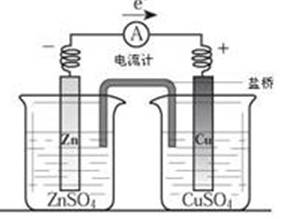
A、铜是阳极,铜片上有气泡产生
B、铜片质量逐渐减少
C、电流从锌片经导线流向铜片
D、铜离子在铜片表面被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化性强弱顺序为BrO3->ClO3->Cl2>IO3->Br2>I2。某同学为验证其中某些离子的氧化性进行如下实验。向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液至过量。
(1)开始滴加KBrO3溶液时的现象为 此时溶液中I-完全被氧化时转移 mol e-。
(2)KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(3)滴加KBrO3溶液至过量时观察到溶液褪色,其可能的原因是(用离子方程式表示)
通过该反应 (填“能”或“不能”)说明碘的非金属性强于溴,原因是 。
(4)若用y表示锥形瓶中含碘物质的物质的量 ,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。

查看答案和解析>>
科目:高中化学 来源: 题型:
 二茂铁分子[Fe(C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右图所示,下列说法正确的是
二茂铁分子[Fe(C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右图所示,下列说法正确的是
A.二茂铁中Fe2+与环戊二烯离子(C5H )之间为离子键
)之间为离子键
B.Fe元素在周期表中的位置是第四周期ⅧA
C.Fe2+的电子排布式为1s22s22p63s23p63d6
D.环戊二烯( )中的碳原子有sp杂化、sp2杂化、sp3杂化
)中的碳原子有sp杂化、sp2杂化、sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是__________________________________________________。

(2)(2012·福建)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:

①在Xm-中,硼原子轨道的杂化类型有____________;配位键存在于________原子之间(填原子的数字标号);m=________(填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有________(填序号)。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
(3)(2012·山东节选)金属镍在电池、合金、催化剂等方面应用广泛。
①过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=________。CO与N2结构相似,CO分子内σ键与π键个数之比为________。
②甲醛(H2C===O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为________________________________________________________________________,
甲醇分子内的O—C—H键角________(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是( )
A.原子最外层电子数:X>Y>Z
B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z-
D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式:__________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为__________,其水溶液与F单质反应的化学方程式为____________________________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显______色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
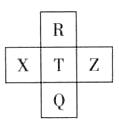 元素R、X、T、Z、Q在元素周期表
元素R、X、T、Z、Q在元素周期表 中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
A.非金属性:Z<T<X
B.R与Q的电子数相差26
C.气态氢化物稳定性:R <T<Q
D.最高价氧化物的水化物的酸性:T>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将0.1 mol·L-1盐酸溶液与0.06 mol·L-1氢氧化钡溶液等体积混合,该混合溶液的pH等于( )
A.1.7 B.2.0 C.12.0 D.12.4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com