
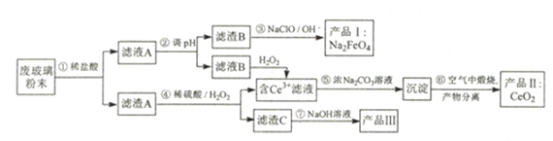
����Ŀ��ƽ�������ʾ�����������л���������ķϲ�����ĩ(��SiO2��Fe2O3��CeO2)�����÷ϲ�����ĩ������ȡ���ֻ�����Ʒ�������������:
�������Ͽ�֪:
��CeO2����:���ƻ�ƺ�ɫ��ĩ��������ˮ�ͼ������;��ǿ�����ԡ�
��Ce3+�ڼ����̼������Һ���������ܵ�̼�Ḵ��Ce2(CO3):Na2CO3��2H2O��
�۳���ʱ���ֳ�������ܶȻ�����:
������ | Fe(OH)3 | Ce(OH)3 |
Ksp | 4.0��10-38 | 1.5��10-20 |
�ش���������:
(1)���̢ٷ���������õ��IJ���������_______________________________��
(2)���̢��з�����Ӧ�����ӷ���ʽΪ_________________________________�����̢��з����Ļ�ѧ��Ӧ����ʽΪ__________________________________��
(3)��ƷI��һ�����͡���ɫ�Ķ�ܾ�ˮ���������������������������������������������Ϊһ�塣��ˮ�����У�Na2FeO4 ���������������õ�ԭ����_________________��
(4)��ҵ��Ҳ���õ��ŨNaOH��Һ�Ʊ���ƷI���������缫��д�����ʱ���������ĵ缫��Ӧ����ʽ_________________��
(5)���������У���ij������Ũ�Ƚ���10��5 mol��L-1ʱ������Ϊ��������ȫ���������̢���Fe3+������ȫʱ��Һ��pH=_____ (��֪ lg2=0.3)��
(6)д����ƷIII��һ����;______________________________________��
���𰸡��ձ���©���������� 2CeO2��H2O2��6H��===2Ce3����4H2O��O2�� 2[Ce2(CO3)3��Na2CO3��2H2O]+O2![]() 4CeO2+2Na2CO3+6CO2��+4H2O ��ˮ�����У�FeO42������ԭ��Fe3+��Fe3+ˮ������Fe(OH)3���壬���������������� Fe��6e��+8OH��=FeO42��+4H2O 3.2 ������ҵ���ϼ���������;��ľ�ġ���֯Ʒ����ʴ������ȼ����
4CeO2+2Na2CO3+6CO2��+4H2O ��ˮ�����У�FeO42������ԭ��Fe3+��Fe3+ˮ������Fe(OH)3���壬���������������� Fe��6e��+8OH��=FeO42��+4H2O 3.2 ������ҵ���ϼ���������;��ľ�ġ���֯Ʒ����ʴ������ȼ����
��������
�����̿�֪����ϲ�����ĩ�м���ϡ���ᣬ�����������ᷴӦ�����Ȼ���������������ϡ�����Ӧ���������沿�������ᷴӦ������˺�����AΪ��������Ͷ������棬��ҺAΪ�Ȼ������Ȼ���Ļ��Һ��������ҺA��pH���Ȼ���ת��Ϊ������������������˺�����BΪ������������ҺBΪ�������Ȼ������Һ�����������£�����������������Ʒ���������ԭ��Ӧ���ɲ�Ʒ��������ƣ������������£�����A�ж����������ҺB�����Ȼ�����˫��ˮ����������ԭ��Ӧ����Ce3�����������費��Ӧ������˺�õ�����Ce3������Һ������CΪ�������裻����Ce3������Һ�м���Ũ̼������Һ����Ӧ����Ce2(CO3)3��Na2CO3��2H2O��Ce2(CO3)3��Na2CO3��2H2O�ڿ������������ɲ�Ʒ��������棻������C�м�������������Һ����������������������Һ��Ӧ���ɲ�Ʒ������ơ�
��1���������ķ������Ϊ���ˣ������õ��IJ����������ձ���©�������������ʴ�Ϊ���ձ���©������������
��2�������������ķ�ӦΪ���������£�����������˫��ˮ����������ԭ��Ӧ����Ce3������Ӧ����Ԫ�ػ��ϼ۽��ͱ���ԭ��������������������˫��ˮ����ԭ������Ӧ�����ӷ���ʽΪ2CeO2��H2O2��6H��=2Ce3����4H2O��O2���������������ķ�ӦΪCe2(CO3)3��Na2CO3��2H2O�ڿ������������ɶ������棬��Ӧ����Ԫ�ػ��ϼ����߱���������������������Ӧ������������Ӧ�Ļ�ѧ����ʽΪ2[Ce2(CO3)3��Na2CO3��2H2O]+O2![]() 4CeO2+2Na2CO3+6CO2��+4H2O���ʴ�Ϊ��2CeO2��H2O2��6H��=2Ce3����4H2O��O2����2[Ce2(CO3)3��Na2CO3��2H2O]+O2
4CeO2+2Na2CO3+6CO2��+4H2O���ʴ�Ϊ��2CeO2��H2O2��6H��=2Ce3����4H2O��O2����2[Ce2(CO3)3��Na2CO3��2H2O]+O2![]() 4CeO2+2Na2CO3+6CO2��+4H2O��
4CeO2+2Na2CO3+6CO2��+4H2O��
��3��Na2FeO4����Ԫ��Ϊ+6�ۣ�����ǿ�����ԣ���ˮ�����У�FeO42����ϸ����ԭ��Fe3+���ﵽɱ�����������ã���Ӧ���ɵ�Fe3+ˮ������Fe(OH)3���壬Fe(OH)3������кܴ�ı�������ܹ�����ˮ���������ʣ����������������ã��ﵽ��ˮ��Ŀ�ģ��ʴ�Ϊ����ˮ�����У�FeO42������ԭ��Fe3+��Fe3+ˮ������Fe(OH)3���壬���������������ã�
��4����ҵ��Ҳ���õ��ŨNaOH��Һ�Ʊ�Na2FeO4ʱ����������ʧ���ӷ���������Ӧ����FeO42�����缫��ӦʽΪFe��6e��+8OH��=FeO42��+4H2O���ʴ�Ϊ��Fe��6e��+8OH��=FeO42��+4H2O��
��5��Fe(OH)3��Ksp=c��Fe3+��c3��OH����=4.0��10-38��Fe3+������ȫʱ��Һ��c��OH����=![]() mol/ L������Һ��pH=14��11+
mol/ L������Һ��pH=14��11+![]() ��lg2=3.2���ʴ�Ϊ��3.2��
��lg2=3.2���ʴ�Ϊ��3.2��
��6����Ʒ��Ϊ�����ƣ���������Һ������������ҵ���ϼ���������;��ľ�ġ���֯Ʒ����ʴ������ȼ���ȣ��ʴ�Ϊ��������ҵ���ϼ���������;��ľ�ġ���֯Ʒ����ʴ������ȼ��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A����ˮ��������ƽ��Br2+H2O![]() HBr+HBrO,��������������Һ��,��Һ��ɫ��dz
HBr+HBrO,��������������Һ��,��Һ��ɫ��dz
B���Ӵ���,ʹN2��H2��һ��������ת��ΪNH3
C����ӦCO(g)+NO2(g)CO2(g)+NO(g) ��H<0,��ƽ���,�����¶���ϵ��ɫ����
D������ѹǿ,������SO2��O2��Ӧ����SO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����ᡢ����������������أ�����˵����ȷ���ǣ� ��
A.![]() �����ڼ���ƾ����Ƿ���ˮ
�����ڼ���ƾ����Ƿ���ˮ
B.![]() ��ָ������ֱ��С�ڻ����
��ָ������ֱ��С�ڻ����![]() �Ŀ������ΰ��������ȼ����ķ���������أ������������������Ҫԭ��
�Ŀ������ΰ��������ȼ����ķ���������أ������������������Ҫԭ��
C.����ˮ����������ˮ����![]() ��
��![]() ���ܴ���������ˮ
���ܴ���������ˮ
D.����ֲ����и��������������˴Ӻ���Ʒ����ȡ���ǹ�ҵ�ϻ�ȡ�����Ҫ;������ҵ�ϴӺ�������ȡ��IJ����У�����![]() ����
����![]() ����
����![]() ��ȡ
��ȡ![]() �ֵ��ᴿ
�ֵ��ᴿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����й�ͭ�����ᡢ���ữѧ���ʵ�ʵ�飬ʵ�������ͼ��ʾ��
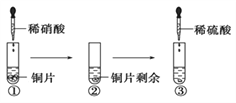
����˵����ȷ����
A. ������Һ����ɫ���Թܿ��к���ɫ���������ϡ���ᱻ��ԭΪNO2
B. ������Һ���ڣ�c(Cu2+) + c(H+) �� c(NO3��) + c(OH��)
C. ������ʵ���ó����ۣ���������Cu�ȿ���ϡ���ᷴӦ��Ҳ����ϡ���ᷴӦ
D. ������Ӧ�Ļ�ѧ����ʽ��3Cu��Cu(NO3)2��4H2SO4 === 4CuSO4 ��2NO����4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������(H2S) �ĵ���ƽ�ⳣ��Ϊ: Ka1(H2S)=9.1��10��8�� Ka2(H2S)=1.1��10 -12��H2S��Һ��c(��)=c(H2S)+c(HS�� )+c(S2�� )����������25.00 mL 0.1000 mol��L��1 'H2S ��Һ����ε���NaOH��Һ������˵����ȷ����
A.����NaOH��Һ���룬��Һ��ˮ�ĵ���̶Ȳ�������
B.c(Na+ )=c(��)����Һ: c(Na +)>c(S2��)> c(H2S)> c(H+)
C.pH=7����Һ: c(Na+)>c(S2��)>c(HS�� )>c(OH�� )=c(H+)
D.c(H+)=9.1��10-8 mol��L-1ʱ: c(H2S)+2c(S2�� )+c(OH�� )=c(Na + )+c(H�� )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A.Fe(OH)3���������(HI)��Fe(OH)3+3H+=Fe3++3H2O
B.��������Ͷ��������ϡ���Fe+4H++NO3-=Fe3++NO��+2H2O
C.��FeBr2��Һ��ͨ�����������2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
D.��FeI2��Һ��ͨ������������2Fe2++Cl2=2Fe3++2Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
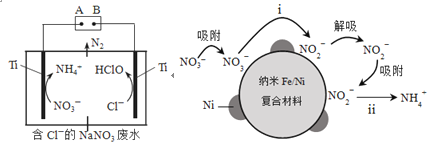
����Ŀ��������Fe/Ni���ϲ�����ȥ����Ⱦˮ���NO3-��Ni�����뷴Ӧ�������ڲ��ϱ���Ļ���λ������������Ӧ������λ�㱻����������ռ�ݻᵼ�����ʼ���(NH4+��ռ�ݻ���λ��)����Ӧ������ͼ��ʾ��
��1�����Ի����У�����Fe/Niȥ��NO3-��������������ii����������
��.NO3-+Fe+2H+=NO2-+Fe2++H2O
��.___+___+___H+=___Fe2++___+___
��2����ʼpH=2.0�ķ�Һ��Ӧ15min���ִ�����ɫ��״����˺�ܿ��ɺ��ɫ����ϻ�ѧ������������仯���̵�ԭ��___��
��3��ˮ���ʼpH��Ӱ�췴Ӧ���ʣ���ͬpH����������Һ������Fe/Ni��Ӧʱ����Һ��![]() ��ʱ��ı仯��ͼ1��ʾ��(ע��c0(NO3-)Ϊ��ʼʱNO3-��Ũ�ȡ�)
��ʱ��ı仯��ͼ1��ʾ��(ע��c0(NO3-)Ϊ��ʼʱNO3-��Ũ�ȡ�)

��Ϊ�ﵽ���ȥ���ʣ�Ӧ��ˮ��ij�ʼpH=___��
��t<15min��pH=2.0����Һ��Ӧ������죬t>15min���䷴Ӧ����Ѹ�ٽ��ͣ�ԭ��ֱ���___��
��4���ܵ���ָ��Һ�������ƶ������к�����Ũ��֮�ͣ�����Fe/Ni����ijŨ����������Һʱ����ʱ��ı仯��ͼ2��ʾ��40minʱ�ܵ����ϳ�ʼʱ�½������ܵ�ԭ����___��

��5�����õ����������ˮ���е�NO3-����������N2�ݳ�����װ�ü�ת��ͼ��ͼ��ʾ��
�������ĵ缫��ӦʽΪ___��
������N2�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ʵ��ܶȻ��������±���
���� | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
����ij����CuCl2��Һ�к���������FeCl2��Ϊ�õ�������CuCl2��2H2O����,����ͼ��������ᴿ��

��1�����ʺ���������X����_________������ĸ��������X��Ŀ����______________��
A��K2Cr2O7B��NaClO C��H2O2D��KMnO4
���������Y��____________���ѧʽ����������ҺpH��4��ʹ��Һ�е�Fe3��ת��ΪFe(OH)3��������ʱ��Һ�е�c(Fe3��)��__________�����˺�������Һ����������Ũ���ᾧ���ɵõ�CuCl2��2H2O���塣
��2��ijѧϰС��������ӵ��������ⶨ����CuCl2��2H2O���������(��������I��������Ӧ������������)�Ĵ��ȣ��������£�ȡ0.36 g��������ˮ���������KI���壬��ַ�Ӧ�����ɰ�ɫ��������0.1000 mol��L-1Na2S2O3����Һ�ζ�������ζ��յ�ʱ������Na2S2O3����Һ20.00mL��(I2��2S2O32-= S4O62-��2I��)
�ٿ�ѡ��___________���ζ�ָʾ����
��CuCl2��Һ��KI��Ӧ�����ӷ���ʽΪ________________��
�۸�������CuCl2��2H2O�������ٷ���Ϊ_______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com