
有一澄清透明的溶液,只可能含有大量的Fe3+、Fe2+、H+、AlO2﹣、Al3+、CO32﹣、NO3﹣七种离子中的几种,向该溶液中逐滴加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,而后才有沉淀.则下列判断正确的是()
A. 溶液中可能含有AlO2﹣
B. 溶液中可能含有NO3﹣
C. 溶液中一定不含Fe2+和Fe3+
D. 溶液中可能含有Fe3+,但一定不含Fe2+
考点: 常见离子的检验方法.
专题: 离子反应专题.
分析: 向该溶液中加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,在酸性溶液中AlO2﹣、CO32﹣离子因发生反应生成弱电解质而不能存在,而后才有沉淀.能够生成沉淀的是Fe3+离子、Fe2+离子或Al3+离子中的一种或几种,结合溶液的电中性和Fe2+离子的还原性以及NO3﹣离子的氧化性做进一步的推断.
解答: 解:向该溶液中加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,
在酸性溶液中AlO2﹣、CO32﹣离子分别与H+离子反应生成Al(OH)3沉淀、CO2气体而不能存在,
根据溶液的电中性可知一定含有阴离子,则只有NO3﹣离子符合;
而后才有沉淀.能够生成沉淀的是Fe3+离子、Fe2+离子或Al3+离子中的一种或几种,但在酸性条件下Fe2+离子与NO3﹣离子发生氧化还原反应而不能共存,则一定不含Fe2+离子,
综上所述,溶液中一定含有H+离子、NO3﹣离子,一定没有AlO2﹣、CO32﹣、Fe2+离子,Fe3+离子、Al3+离子至少有一种.
故选D.
点评: 本题考查常见离子的检验,注意从反应的现象推断离子的存在性,把握物质的性质和离子的检验方法是做本题的关键,题目难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
下列离子方程式正确的是()
A. 三氯化铝溶液中加入过量氨水:Al3++3OH﹣═Al(OH)3↓
B. 向含有0.2 mol FeI2的溶液中通入0.25 mol Cl2:8I﹣+2Fe2++5Cl2═10Cl﹣+4I2+2Fe3+
C. K37ClO3与浓盐酸(HCl)在加热时生成Cl2:37ClO3﹣+6HCl═37Cl﹣+3Cl2↑+3H2O
D. 将0.1 mol/L盐酸数滴缓缓滴入0.1 mol/L 25 mL Na2CO3溶液中,并不断搅拌:2H++CO32﹣═CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列物质,正盐:钾盐、钠盐、铵盐、钡盐;酸:盐酸、硝酸、醋酸、稀硫酸.在水溶液中符合离子方程式:2H++CO32﹣═CO2↑+H2O的化学反应的组合共有()
A. 6个 B. 9个 C. 12个 D. 15个
查看答案和解析>>
科目:高中化学 来源: 题型:
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,同温下测得容器内压强不变,且反应后气体C的密度是原气体密度的4倍.则下列判断正确的是()
A. 两种单质的摩尔质量比为1:4
B. 生成物C中A的质量分数为75%
C. 生成物C中A、B的原子个数比为3:1
D. 反应前后气体分子数比为1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A. “血液透析”利用了胶体的性质
B. 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C. 明矾能水解生成Al(OH)3胶体,可用作净水剂
D. 依据丁达尔现象可将分散系分为溶液、胶体与浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42﹣)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0g,若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
A. 9.0 L B. 13.5 L C. 15.7 L D. 16.8 L
查看答案和解析>>
科目:高中化学 来源: 题型:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为 。
(2)该小组同学将2.52g草酸晶体(H2C2O4∙2H2O)加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性(忽略溶液体积变化),则下列关系合理的是 。
A.c(Na+) +c(H+) =c(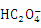 ) +c(OH-) +c(
) +c(OH-) +c(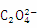 )
)
B.c(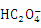 ) +c(
) +c(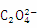 ) =0.2 mol/L
) =0.2 mol/L
C.c(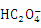 )>c(
)>c(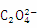 ) >c(H2C2O4)
) >c(H2C2O4)
D.c(Na+)= c(H2C2O4) +c(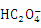 ) +c(
) +c(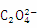 )
)
(3)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,有气泡产生,说明乙二酸具有 (填“还原性”、“氧化性”或“酸性”),请写出该反应的离子方程式: 。
(4)乙二醇与乙二酸类似,每个碳上连一个羟基。现以乙烯为原料(其他无机试剂任选),写出由乙烯合成乙二醇的化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com