
已知A、B、C、D、E都是周期表中前四周期的元素,且原子序数依次增大,其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)比E核外电子数少5的元素的原子核外电子排布式是________________,A、B、C、D的第一电离能由小到大的顺序为________________。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是
 ________________________________。
________________________________。
(3)A的氢化物属于________(填“极性”或“非极性”)分子,D的低价氧化物分子的空间构型是_____________________________________________。
(4)A、E形成的某种化合物的晶胞结构如图所示,则其
化学式为__________(每个球均表示1个原子)。
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
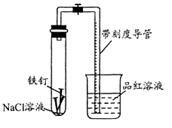
常温下,某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。
(1) 实验前用碱液清洗铁钉,再用0.100mol/L的 H2SO4溶液浸泡至有气泡产生。用H2SO4溶液浸泡的目的是______。
(2) 为尽量减小误差,下列操作的正确顺序是______(填序号)。
①装入铁钉
②插入注射器向铁钉表面滴入适量 NaCl溶液并打开止水夹
 ③将导管口浸入品红溶液
③将导管口浸入品红溶液
④塞上单孔活塞
⑤检查装置气密性
(3) 检查装置气密性的方法:_______________________________。
(4)实验中试管内发生的反应为:____________________________。
用该实验方案测量空气中O2的体积百分数时应测量的数据是:①导管与试管内部空间总体积,
②__________________________________________。
(5) 实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析:
假设一:电解质溶液的PH 假设二: NaCl溶液的浓度 假设三:铁钉的表面积
(6)借助上述实验装置,通过调节溶液的pH验证假设一,获得了如下实验数据:
①当pH=2时,没有观察到稳定液柱形成的原因是______
②根据实验数据分析,为缩短实验测定时间,pH的最佳范围是______
③按上述实验装置,设计实验证明假设二。
第一步:____________;
第二步: ______,分别用注射器将NaCl溶液滴入铁钉表面;
第三步:记录形成稳定液柱所用时间和液柱的高度,比较分析数据得出结论。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;
②2CH3CHO+O2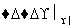 2CH3COOH。
2CH3COOH。
现以A为主要原料合成乙酸乙酯,其合成路线如图CB33所示。
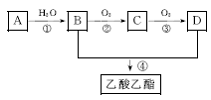
图CB33
回答下列问题:
(1)写出A的电子式:____________________。
(2)B、D分子中的官能团名称分别是__________、__________。
(3)写出下列反应的反应类型:①___________反应,②___________反应,④________反应。
(4)写出下列反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述中正确的是 ( )。
A.CS2为V形的极性分子
B.ClO3-的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO32-的中心原子均为sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
二氯化硫(Cl—S—S—Cl,直线形)是一种琥珀色液体,是合成硫化染料的重要原料。
(1)写出它的电子式 。
(2)指出它分子内的键型 。
(3)估计它是否易溶于水 。
(4)指出硫元素的化合价为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是 ( )。
A.用盐的形式表示:BaSiO3·CuSiO3
B.用氧化物形式表示:BaO·CuO·2SiO2
C.易溶于强酸、强碱
D.性质稳定,不易褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
|
| A. | 需加热才能发生的反应一定是△H>0 |
|
| B. | CaCO3(s)受热分解为CaO(s)和CO2(g)反应的△S<0 |
|
| C. | 1 mol H2SO4与1 mol Ba(OH)2反应放出的热就是中和热 |
|
| D. | 热化学方程式中的化学计量数表示物质的量,所以可以是分数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com