
【题目】化学与生活密切相关。下列说法不正确的是
A. 乙烯可作水果的催熟剂
B. 硅胶可作袋装食品的干燥剂,铁粉可做脱氧剂
C. 福尔马林可作食品的保鲜剂
D. 氢氧化铝可作胃酸的中和剂
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是
。有关该物质的下列说法正确的是
A. 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物有6种
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去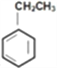 中的苯乙烯可以通入等量氢气反应
中的苯乙烯可以通入等量氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 吸热反应在一定条件下也可以发生
B. 需要加热才能发生的反应不一定是吸热反应
C. 反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
D. 放热反应在常温下一定很容易发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系:mA(g)+ nB(g)![]() pC(g)+ qD(g),下列判断正确的是( )
pC(g)+ qD(g),下列判断正确的是( )
A.若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.55 倍,则m+n<p+q
B.若升高平衡体系的温度,达到新平衡时A 的浓度变为原来的0.55 倍,说明该反应△ H<0
C.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
D.若平衡后同时增大A、B的浓度,则A、B的转化率一定都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知五种短周期元素在周期表中的相对位置如图所示。
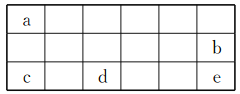
(1)表中五种元素金属性最强的元素为_______(填元素符号),c、e两元素形成的离子化合物c2e的电子式为___________。
(2)c、d、e三种元素的简单离子中,半径最小的是________(用元素符号表示)。
(3)b、e两元素分别与a形成的最简单气态化合物的稳定性的关系为____________(用化学式表示)。
(4)已知A、B、C、D、E、F六种化合物均由上述元素中的几种组成。它们之间的关系如图所示,A为淡黄色固体,B是常见液体,D是两性氧化物,F是引起酸雨的主要气体。
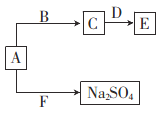
①写出物质E的化学式:_________。
②写出A与F反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
(1)在通常状况下,金刚石和石墨相比较, (填”金刚石”或”石墨”)更稳定,石墨的燃烧热为 。

(2)12 g石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量为 。
Ⅱ、磷在氧气中燃烧,可能生成两种固态氧化物P2O3和P2O5 , P2O5在通常状态下稳定。已知3.1 g的单质磷(P)在3.2 g氧气中燃烧,至反应物耗尽,放出X kJ热量。
(3)写出两种磷的氧化物对应的质量(g)为 、 。
(4)已知单质磷的燃烧热为Y kJ/mol,写出1mol P与O2反应生成固态P2O3的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国丝绸有五千年的历史和文化,古代中国丝绸有五千年的历史和文化。古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层的丝胶蛋白质水解而除去,使丝绸颜色洁白、质感柔软、色泽光亮。这种“碱剂”可能是
A. 食盐 B. 火碱 C. 草木灰 D. 胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用某种仪器量一液体体积时,平视读数为 V1mL,仰视读数为 V2mL,俯视读数为 V 3 mL, 若 V 3 >V 1>V 2,则所使用仪器可能是( )
A.容量瓶 B.量筒 C.碱式滴定管 D.以上仪器均可
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种高能燃料,也广范应用在工业合成中。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1 mol化合物的焓变。已知25℃和101kPa时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H=-3116kJ·mol-1
②C(石墨,s)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+02(g)=2H2O(l),△H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:_____________。
(2)已知合成氨的反应为:N2+3H2![]() 2NH3 △H <0。某温度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H <0。某温度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是______(用a、b、c表示)。
②曲线a条件下该反应的平衡常数K=__________________。
③b容器中M点,v(正)_____ v(逆)(填“大于”、“小于”.或“等于”)。
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为_____;标准状况下,当阴极收集到1l.2LN2时,理论上消耗NH3的体积为_______。
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s)![]() Cu2++2OH- Ksp=2.2×10-20
Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O![]() [Cu(NH3)4]2+(深蓝色)+4H2O Kβ=7.24×1012
[Cu(NH3)4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s)+4NH3·H2O![]() [Cu(NH3)4]2++4H2O+2OH- 配制铜氨溶液是否可行:________________。
[Cu(NH3)4]2++4H2O+2OH- 配制铜氨溶液是否可行:________________。
②已知反应Cu(OH)2(s)+2NH3·H2O+2NH4+![]() [Cu(NH3)4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol/L的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为__________;解释出现该现象的原因是_____________________。
[Cu(NH3)4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol/L的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为__________;解释出现该现象的原因是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com