
【题目】下列物质中均既有离子键又有共价键的一组是
A.NaOH、H2O、NH4ClB.KOH、Na2O2、NH4Cl
C.MgO、CaBr2、NaClD.Na2S、HCl、MgCl2
科目:高中化学 来源: 题型:
【题目】化合物G是一种医药中间体,常用于制备抗凝血药。可以通过如图所示的路线合成:
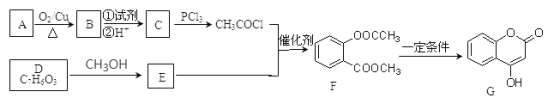
已知:①RCOOH![]() RCOCl;②D与FeCl3溶液能发生显色反应。
RCOCl;②D与FeCl3溶液能发生显色反应。
③:![]()
回答下列问题:
(1)C→H的反应类型是_______________,B→C步骤①中所加的试剂可能是_____________,D中的官能团名称为____________________。
(2)B、E的结构简式为:B:_____________,E:______________。
(3)A→B的化学方程式为_________________,G与足量NaOH溶液充分反应的化学方程式为_________________________。
(4)写出同时满足下列条件的所有E的同分异构体的结构简式________________。
①不能发生水解反应,能发生银镜反应
②该分子核磁共振氢谱有五个组峰,且峰面积之比为2:2:2:1:1
③与FeCl3溶液能发生显色反应
④苯环上有两种不同化学环境的氢原子
(5)已知:酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(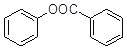 )是一种重要的有机合成中间体。试结合题中信息写出以苯酚、甲苯为原料制取该化合物合成路线流程图(其他试剂任选)______。合成路线流程图示例:
)是一种重要的有机合成中间体。试结合题中信息写出以苯酚、甲苯为原料制取该化合物合成路线流程图(其他试剂任选)______。合成路线流程图示例: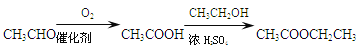
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过CO传感器可监测CO的含量,总反应为2K2FeO4+3CO+2KOH+2H2O=2Fe(OH)3+3K2CO3,其工作原理示意图如下,下列说法正确的是
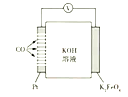
A. 电极为负极,可以用Fe电极代替
B. 工作时OH-向K2FeO4电极移动
C. 每转化3molCO,有2molK2FeO4被氧化
D. K2FeO4电极上的电极反应式是2FeO42-+8H2O+6e-=2Fe(OH)3↓+10OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,X与M同主族,Z的气态氧化物能与其最高价氧化物的水化物反应,G是地壳中含量最高的金属元素。清回答下列问题:
(1)Q的元素符号为______,Y、Z、M、G四种元素原子半径由大到小的顺序是(写元素符号)___________。
(2)Y在元素周期表中的位置为_______________,Y与硫元素形成的二元化合物的电子式为_________________________。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)____________________。
(4)单质Y和元素Z的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为_________。
(5)Z和G组成的化合物GZ,被大量用于制造电子元件。工业上用G的氧化物、Y单质和Z单质在高温下制备GZ,其中G的氧化物和Y单质的物质的量之比为1:3,则该反应的化学方程式为__________________________。
(6)常温下,不能与G的单质发生反应的是(填序号)_________________________。
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为 。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为 (填化学式)。
③NaH2PO2为 (填“正盐”或“酸式盐”)
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系。
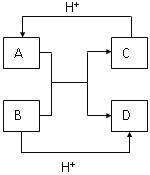
(1)如果A、B、C、D均是10电子微粒,请写出A的化学式:___________;D的化学式__________。
(2)如果A和C是18电子的微粒,B和D是10电子的微粒,请写出A与B在溶液中反应的离子方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2 溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为:2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示:
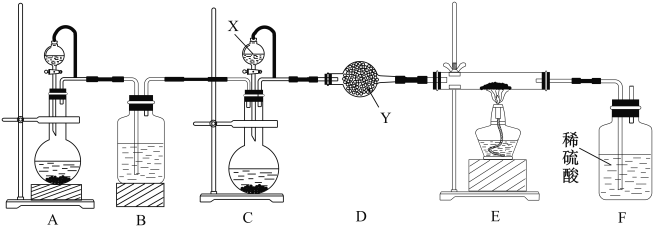
设计实验步骤如下:
①滴加几滴NiCl2 溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间后的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应过滤、洗涤、干燥。
(1)仪器X中的试剂是___________,仪器Y的名称是__________________。
(2)指出该套装置中存在一处明显的错误是________________________。
(3)步骤①中选择NiCl2 溶液,不选择氧化镍的原因是____________________。
a.增大接触面积,加快化学反应速率
b使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时观察到的现象是____________________。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作________________________。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热NaOH溶液的离子方程式:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com