
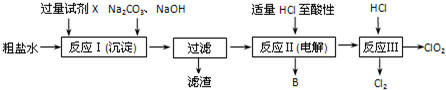
���� ��1����ʳ��ˮ�к���Ca2+��Mg2+��SO42-�����ʣ����Ӳ���ʱ��������ˮ���ȼ���������Լ�BaCl2�����ڳ�ȥSO42-�����������ٲ������ټ��������Na2CO3����ȥԭ��Һ�е�Ca2+��Ϊ��ȥSO42-�������Ba2+��Ȼ���ټ���NaOH��Һ����ȥMg2+����ַ�Ӧ����һ����ȥ������ⷢ����Һ���Ժ���һ������SO42-������Ϊ����Һ�г����ܽ�ƽ�⣬BaSO4 ��BaCO3��Ksp������Һ�д��ڴ�����CO32-����ʱ��BaSO4��s���Ჿ��ת��ΪBaCO3��s����
��2����ʳ��ˮ���ض������µ��õ��������ƣ�����������ԭ��Ӧ�еĻ��ϼ������뽵�͵���������жϵ��ʱ���ɵ�����B�����ƣ��������ⷴӦ��Ϊ���������Ȼ��ⷴӦ���ɶ������ȡ��Ȼ��ƺ�ˮ��
��3����ClO2��Һ�����ԣ�Ӧ������ʽ�ζ���ȷ��ȡ10.00 mL ClO2��Һ��
��Ϊ�˼���ʵ���żȻ�ԣ�����ʵ����ʵ��������ƽ�вⶨ���Σ�ȡ��ƽ��ֵ��
���ɷ���ʽClO2+I-+H+-I2+Cl-+H2O��I2+2S2O32-�T2I-+S4O62-�ù�ϵʽClO2��5S2O32-��n��S2O32-��=cV2��10-3mol������V1mL ClO2����Һ�к��е�ClO2�����ʵ���Ϊ2cV2��10-4mol������c=$\frac{n}{V}$�����ԭClO2��Һ�����ʵ���Ũ�ȣ�
��� �⣺��1�����Ӳ���ʱ��������ˮ���ȼ���������Լ�BaCl2�����ڳ�ȥSO42-�����������ٲ������ټ��������Na2CO3����ȥԭ��Һ�е�Ca2+��Ϊ��ȥSO42-�������Ba2+��Ȼ���ټ���NaOH��Һ����ȥMg2+����ַ�Ӧ����һ����ȥ������ⷢ����Һ���Ժ���һ������SO42-������Ϊ����Һ�г����ܽ�ƽ�⣬BaSO4 ��BaCO3��Ksp������Һ�д��ڴ�����CO32-����ʱ��BaSO4��s���Ჿ��ת��ΪBaCO3��s����
�ʴ�Ϊ��BaCl2��BaSO4��BaCO3��Ksp������Һ�д��ڴ�����CO32-����ʱ��BaSO4��s���Ჿ��ת��ΪBaCO3��s����
��2����ʳ��ˮ���ض������µ��õ��������ƣ�����������ԭ��Ӧ�еĻ��ϼ������뽵�͵�������ȿ�֪���ʱ���ɵ�����BΪH2���������ⷴӦ��Ϊ���������Ȼ��ⷴӦ���ɶ������ȡ��Ȼ��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��2NaClO3+4HCl�T2ClO2��+2NaCl+2H2O��
�ʴ�Ϊ��H2��2NaClO3+4HCl�T2ClO2��+2NaCl+2H2O��
��3����ClO2��Һ�����ԣ�����ȷ��ȡ10.00 mL ClO2��Һ�IJ�����������ʽ�ζ��ܣ�
�ʴ�Ϊ����ʽ�ζ��ܣ�
���ڼ��Եζ�ʵ�����������������Ϊ�˼���ʵ���żȻ�ԣ�����ʵ����ʵ��������ƽ�вⶨ���Σ�ȡ��ƽ��ֵ���������ӽ�����ֵ��
�ʴ�Ϊ������ʵ����
���ɷ���ʽClO2+I-+H+-I2+Cl-+H2O��I2+2S2O32-�T2I-+S4O62-�ù�ϵʽClO2��5S2O32-��n��S2O32-��=cV2��10-3mol������V1mL ClO2����Һ�к��е�ClO2�����ʵ���Ϊ2cV2��10-4mol����10mL��ԭ��Һ����ClO2�����ʵ���Ϊ��2cV2��10-4mol��$\frac{100mL}{{V}_{1}}$=$\frac{2c{V}_{2}}{{V}_{1}}$��10-2mol������ԭClO2��Һ�����ʵ���Ũ��Ϊ��$\frac{\frac{2c{V}_{2}}{{V}_{1}}��1{0}^{-2}mol}{0.01L}$=$\frac{2c{V}_{2}}{{V}_{1}}$mol/L��
�ʴ�Ϊ��$\frac{2c{V}_{2}}{{V}_{1}}$��
���� ���⿼��������ʵ�鷽������ơ���ѧʵ������������������ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ���ȷʵ��ԭ������ѧʵ�������������Ϊ���ؼ��������ۺ��Խ�ǿ����ֿ�����ѧ���ķ������������������Ӧ�û���֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢݢ�� | B�� | �ڢܢݢߢ� | C�� | �٢ۢޢ�� | D�� | �ۢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C3N4������ԭ�Ӿ��� | |
| B�� | C3N4�����У�C-N���ļ����Ƚ��ʯ�е�C-C���ļ���Ҫ�� | |
| C�� | C3N4������ÿ��Cԭ������4��Nԭ�ӣ���ÿ��Nԭ������3��Cԭ�� | |
| D�� | C3N4����������ͨ�����Ӽ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ΪFe3O4��SiO2 | |
| B�� | �������뻹ԭ�����ʵ�����֮��Ϊ2��3 | |
| C�� | ����1.5mol Fe2SiO4�μӷ�Ӧʱ��ת�Ƶĵ���Ϊ3 mol | |
| D�� | ����1mol CO2�μӷ�Ӧʱ����������Fe2SiO4�����ʵ���Ϊ1mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ѹǿ/Mpa ת����/% �¶�/�� | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ʼ������pH | ������ȫ��pH | |
| Fe3+ | 1.1 | 3.2 |
| Mg2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��ѧʵ��С����Ҫ�˽��г�������ʳ�ð״ף���Ҫ�Ǵ����ˮ��Һ����Ũ�ȣ��ִ��г�������һƿijƷ��ʳ�ð״ף���ʵ���ұ�NaOH��Һ������еζ����±���4�ֳ���ָʾ���ı�ɫ��Χ��
ij��ѧʵ��С����Ҫ�˽��г�������ʳ�ð״ף���Ҫ�Ǵ����ˮ��Һ����Ũ�ȣ��ִ��г�������һƿijƷ��ʳ�ð״ף���ʵ���ұ�NaOH��Һ������еζ����±���4�ֳ���ָʾ���ı�ɫ��Χ��| ָʾ�� | ʯ�� | ���� | ���� | ��̪ |
| ��ɫ��Χ��pH�� | 5.0��8.0 | 3.1��4.4 | 4.4��6.2 | 8.2��10.0 |
| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ����NaOH��Һ���/mL | 26.02 | 25.32 | 25.28 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1��NaHSO3��Һ��0.2 mol•L-1��NaClO��Һ�������ϣ�HSO3-+ClO-=SO42-+Cl-+H+ | |
| B�� | ��Ũ�ȵ�Fe2��SO4��3��Һ��Ba��OH��2��Һ��ϣ�2Fe3++3SO42-+3Ba2++6OH-=2Fe��OH��3��+3BaSO4�� | |
| C�� | Ca��HCO3��2��Һ������NaOH��Һ��Ӧ��2HCO3-+Ca2++2OH-=CaCO3��+CO32-+2H2O | |
| D�� | H218O��Ͷ��������ƣ�2H218O+2Na2O2=4Na++4OH-+18O2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com