
X、Y、Z是中学化学常见的三种元素,其中,X、Z位于短周期.常温下,X单质为黄绿色气体;向含Y离子的溶液中滴加氢氧化钠溶液,生成白色絮状沉淀,迅速变为灰绿色,最后变为红褐色;Z的最外层电子数与核外电子总数之比为3∶13.请回答下列问题:
(1)Z在元素周期表中的位置是________,X单质分子的电子式是________.
(2)Z单质与Y的氧化物在高温条件下反应是冶炼Y单质的一种方法,该反应化学方程式是________.
(3)含上述元素的某些物质常用于处理工业废水,部分流程如下图:

①处理含铬废水时,在反应池中Cr2O![]() 变为Cr3+,当反应转移1 mol电子时,有________mol Cr2O
变为Cr3+,当反应转移1 mol电子时,有________mol Cr2O![]() 转化(计算结果保留两位小数).
转化(计算结果保留两位小数).
②含Z化合物可以使水中悬浮颗粒发生凝聚,原因是________________(用文字和化学用语表示).
③处理含氰废水时,CN-最终转化为两种无毒的气体,该反应的离子方程式是________.
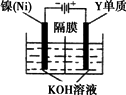
(5)利用下图方法电解可得到一种新型净水剂K2YO4,阳极的电极反应式为________.
科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |

查看答案和解析>>
科目:高中化学 来源: 题型:
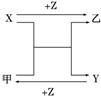 X、Y、Z是中学化学中三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系(未注明反应条件),下列说法不正确的是( )
X、Y、Z是中学化学中三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系(未注明反应条件),下列说法不正确的是( )| A、若X为金属单质,Y为非金属固体单质,则Z为O2 | B、若X、Y均为金属单质,则甲不可能为黑色固体 | C、若X为金属单质,Y为非金属气体单质,则乙可能为黑色固体 | D、若X、Y均为非金属固体单质,则Z可能为O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z中,只有Y能使湿润的淀粉碘化钾试纸变蓝 | B、1mol Y或Z与足量水完全反应时,均转移2mol电子 | C、Z为离子化合物,但含有非极性键,阴、阳离子个数比为1:2 | D、X和Y均能用向上排空气法和排水法收集 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com