
【题目】下列有关检测生物组织中糖类、脂肪和蛋白质实验的叙述,正确的是
A. 斐林试剂的甲液与双缩脲试剂的A液的化学成分是相同的
B. 还原糖和蛋白质的鉴定过程都需要水浴加热
C. 检测生物组织中的还原糖时可采用西瓜汁作材料
D. 检测花生子叶中的脂肪实验时,可用稀盐酸洗去浮色
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列描述正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.40gNaOH溶解在1L水中,所制得的溶液,物质的量浓度为1molL﹣1
C.标准状况下,11.2L四氯化碳所含分子数为0.5NA
D.常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是 ( )
A.三氯蔗糖(C12H19Cl3O8)属于天然的糖类甜味剂
B.未成熟的青苹果肉遇碘酒变蓝色,成熟苹果的汁能发生银镜反应
C.利用盐析的方法可以用来分离、提纯蛋白质
D.酚醛树脂、合成橡胶、有机玻璃都属于有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)H﹣H、O = O和O﹣H键的键能分别为: a kJ/mol、b kJ/mol和c kJ/mol。CH3OH(g)的燃烧热为△H=—d kJ/mol。则CO2(g)+3H2(g) = CH3OH(g)+ H2O(l) △H= kJmol﹣1。(用含a、b、c、d的代数式表示)
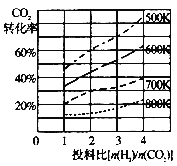
(2)将CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(l)
CH3OCH3(g)+3H2O(l)
已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示。该反应的△H 0(填“>”或“<”)。若温度不变,减小反应投料比,K值将 (填“增大”、“减小”或“不变”)。
(3)某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生反应制备二甲醚,当下列物理量不再发生变化时,能表明上述可逆反应达到化学平衡的是 。(填字母,多选)
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比
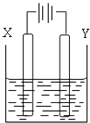
(4)以二甲醚、空气、KOH溶液组成的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,如图所示,请写出该燃料电池负极反应式 。当燃料电池消耗2.8LO2(标况)时,NaCl溶液的pH= (溶液体积变化忽略)(常温)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,试管中各有10 mL相同浓度的盐酸(如下图),同时将两个侧管中的物质 全部倒入各自的试管中,下列叙述正确的是

A.甲装置的气球膨胀速率大
B.若最终两气球体积相同,则一定有c(HCl)≥2molL-1
C.若最终两气球体积不同,则一定有c(HCI)≤lmolL-1
D.最终两溶液中Na+、C1-的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量小
C.气体体积:甲>乙
D.甲的相对分子质量比乙的相对分子质量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
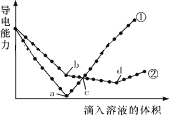
A.②代表滴加H2SO4溶液的变化曲线
B.b点溶液中大量存在的离子是SO42-、Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点两溶液中含有相同量的OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业上,合成氨与制备硝酸一般可连续生产,流程如下:

(1)合成塔中发生反应N2(g)+3H2(g)![]() 2NH3(g)△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1___________300℃(填“>”、“<”或“=”)。
2NH3(g)△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1___________300℃(填“>”、“<”或“=”)。
![]()
(2)氨气在纯氧中燃烧,生成一种单质和水,科学家利用此原理,设计成氨气—氧气燃料电池,电解质溶液为KOH,则负极电极发生反应的电极反应式为___________________。
(3)在80℃时,将铜与浓硝酸反应得到的0.40mol N2O4气体充入2L已经抽空的固定的密闭容器中发生反应N2O4 (g)![]() 2NO2(g),△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g),△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:

①计算a=_________,此温度时该反应的平衡常数K=____________;
②改变条件使反应重新达到平衡,能使c(NO2)/c(N2O4)值变小的措施有___________(填序号)。
A.增大N2O4的起始浓度 B.升高温度 C.使用高效催化剂 D.向混合气体中通入稀有气体
(4)硝酸厂的尾气直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷将氮的氧化物还原为氮气和水,反应机理为:CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) △H=﹣574kJmol﹣1
4NO(g)+CO2(g)+2H2O(g) △H=﹣574kJmol﹣1
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) △H=﹣1160kJmol﹣1
2N2(g)+CO2(g)+2H2O(g) △H=﹣1160kJmol﹣1
则甲烷直接将NO2还原为N2的热化学方程式为:____________________ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com