
.(16分)Ⅰ.已知下列反应的热化学方程式为:
(1) C(s) + O2(g) = CO2(g) △H1 = -393.5 kJ/mol
(2) CH3COOH(l) + 2O2(g) = 2CO2(g) + 2H2O(l) △H2 = -870.3 kJ/mol
(3) 2H2(g) + O2(g) = 2H2O(l) △H3 = -571.6 kJ/mol
请计算:2C(s) + 2H2(g) + O2(g)= CH3COOH(l) △H4 = 。
Ⅱ.在某温度下,物质(t-BuNO)2在正庚烷或CCl4溶剂中均可以发生反应:
(t-BuNO)2  2(t-BuNO) 。该温度下该反应在CCl4溶剂中的平衡常数为1.4。
2(t-BuNO) 。该温度下该反应在CCl4溶剂中的平衡常数为1.4。
(1)向1L正庚烷中加入0.50mol(t-BuNO)2,10min时反应达平衡,此时(t-BuNO)2的平衡转化率为60%(假设反应过程中溶液体积始终为1L)。反应在前10min内的平均速率为ν(t-BuNO)= 。列式计算上述反应的平衡常数K = 。
(2)有关反应:(t-BuNO)2  2(t-BuNO) 的叙述正确的是( )
2(t-BuNO) 的叙述正确的是( )
A.压强越大,反应物的转化率越大 B.温度升高,该平衡一定向右移动
C.溶剂不同,平衡常数K值不同
(3)通过比色分析得到40℃时(t-BuNO)2和(t-BuNO)浓度随时间的变化关系的几组数据如下表所示,请在同一图中绘出(t-BuNO)2和(t-BuNO)浓度随时间的变化曲线。

时间(min) | 0 | 1 | 3 | 5 | 7 | 9 | 11 |
c(t-BuNO)2 mol/L | 0.05 | 0.03 | 0.01 | 0.005 | 0.003 | 0.002 | 0.002 |
c(t-BuNO) mol/L | 0 | 0.04 | 0.08 | 0.07 | 0.094 | 0.096 | 0.096 |
Ⅲ.甲醇燃料电池的电解质溶液是KOH溶液。则通甲醇的电极反应式为 。若通空气的电极上有32g O2参加反应,则反应过程中转移了 mol e-。
31.(16分)Ⅰ.-488.3kJ/mol (3分,没写单位扣1分)
Ⅱ.(1)ν(t-BuNO)=0.06mol?L-1?min-1 (2分,没写或写错单位扣1分)
【解析】
当(t-BuNO)2的起始浓度(c0)为0.50mol?L-1时,实验测得平衡转化率(α)是60%,
则(t-BuNO)2  2(t-BuNO)
2(t-BuNO)
开始浓度(mol?L-1) 0.5 0
转化浓度(mol?L-1) 0.5×60% 0.5×60%×2 (过程1分)
平衡浓度(mol?L-1) 0.5×(1-60%) 0.5×60%×2
(或只写这个也2分) K=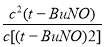 =
=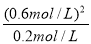 =1.8(2分)
=1.8(2分)
(2)C (2分)
(3)(2分,每条线1分,提示t-BuNO在第5min的数据
要处理掉)

Ⅲ.CH3OH + 8OH- -6 e-= CO32- + 6H2O(2分) 4 (2分)
【解析】
试题分析: Ⅰ.根据盖斯定律,目标方程式可由已知方程式=(1)×2+ (3) -(2),所以△H4 =2△H1+△H3-△H2 =-488.3kJ/mol。
II.(1)此题中正庚烷和CCl4均是溶剂,不参加反应,因此根据反应的方程式就可以列式计算反应的平均反应速率和平衡常数K如下:
【解析】
当(t-BuNO)2的起始浓度(c0)为0.50mol?L-1时,实验测得平衡转化率(α)是60%,
则(t-BuNO)2  2(t-BuNO)
2(t-BuNO)
开始浓度(mol?L-1) 0.5 0
转化浓度(mol?L-1) 0.5×60% 0.5×60%×2 (过程1分)
平衡浓度(mol?L-1) 0.5×(1-60%) 0.5×60%×2
ν(t-BuNO)=△C(t-BuNO)/ △t=0.5 mol?L-1×60% ×2/10min=0.06mol?L-1?min-1
K=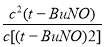 =
=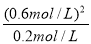 =1.8(2分)
=1.8(2分)
(2)该反应是在溶液中进行的,没有气体参加反应,因此压强不能够改变反应的平衡,A错误;该反应没有告诉焓变的大小,因此不能判断反应是吸热还是放热,因此升高温度不能确定平衡移动方向,B错误;而根据(1)中算得的相同温度下在正庚烷作溶剂的溶液中反应的K的大小为1.8,大于CCl4作溶剂时的K值1.4,因此能够说明该反应在不同溶剂的作用下,平衡常数值不同,故选C。
(3)表中给出的是不同时刻可逆反应的反应物和生成物的浓度大小,根据经验判断,随着反应的进行,反应物不断减少,生成物倍数关系增加,,各物质的量增加慢慢趋于平缓,最终达到平衡,量保持不变。因此把表中的数据全部带入时,会发现5min的点明显跟反应的趋势存在较大差异,因此该时刻的数据不能使用,应舍弃。所以作出的图像如图。

Ⅲ.甲醇做碱性燃料电池时,甲醇在负极发生失电子的反应并且和碱反应生成了CO32-,因此电极反应式为:CH3OH + 8OH- -6 e-= CO32- + 6H2O。通空气的一端为正极,氧气得到电子被还原,一个O2分子得到4个电子,因此32g氧气反应应该转移4mol电子。
考点:本题考查的是


科目:高中化学 来源:2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷(解析版) 题型:选择题
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
A.在自然界中只以化合态的形式存在
B.单质常用作半导体材料和光导纤维
C.最高价氧化物不与酸反应
D.气态氢化物比甲烷稳定
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省、揭阳一中两校届高三5月三模化学试卷(解析版) 题型:填空题
(16分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程如下:
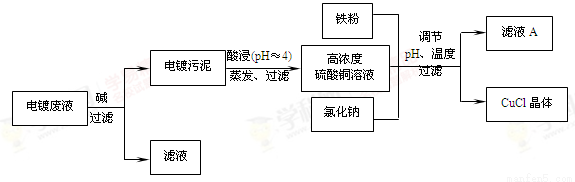
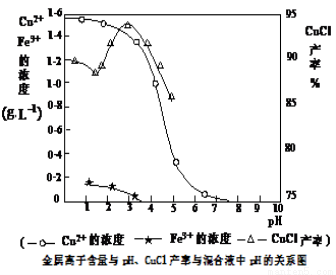
请回答下列问题:
(1)电镀污泥的主要成分是 (写化学式)。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
。
(3)析出CuCl晶体时的最佳pH在 左右。
(4)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是 。
(5)从滤液A中可回收的主要物质是 (写化学式)。
(6)以碳棒为电极电解CuCl2溶液可得到CuCl。写出电解CuCl2溶液后的阴极上发生的反应为
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高一下学期期末考试化学试卷(解析版) 题型:选择题
mA(s)+nB(g) qC(g)的可逆反应中,图甲在恒温条件达平衡时,B的体积分数(B%)与压强(p)的关系,图乙表示在一定条件下达到平衡(v正=v逆)后t1时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,有关叙述正确的是
qC(g)的可逆反应中,图甲在恒温条件达平衡时,B的体积分数(B%)与压强(p)的关系,图乙表示在一定条件下达到平衡(v正=v逆)后t1时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,有关叙述正确的是
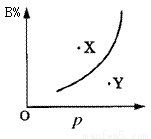
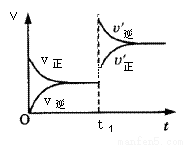
甲 乙
A.n<q B.n>q
C.正反应为放热反应 D.X点比Y点反应速率快
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有关叙述中正确的是
A.难溶于水的电解质一定是弱电解质
B.强电解质在水溶液中的电离过程是不可逆的
C.易溶于水的电解质一定是强电解质
D.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省湛江市高三年级第二次模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.铝合金的熔点比纯铝高
B.电解MgCl2溶液可获得金属镁
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.铜具有良好的导电性,常用来制作印刷电路板
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省第一学期期终考试高一级化学科试卷甲卷(解析版) 题型:实验题
实验室可以用如下方法制取少量单质溴:
2NaBr+MnO2+2H2SO4 Na2SO4+MnSO4+Br2↑+2H2O
Na2SO4+MnSO4+Br2↑+2H2O
根据左图实验装置,填空和回答问题:

(1)装置(Ⅰ)的烧杯中冷水所起的作用是______ ,装置(Ⅱ)的烧杯中液体的作用是 ______________。
(2)进行此实验时,烧瓶内的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为 ____________________________。
(3)装置(Ⅱ)烧杯中使用倒置漏斗可防止液体倒吸,试简述其原因
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省第一学期期终考试高一级化学科试卷甲卷(解析版) 题型:选择题
与22g CO2所含分子数相等的水的质量是
A.44g B.22g C.18g D.9g
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高考预测理综化学试卷二(解析版) 题型:填空题
(本题16分)已知反应①:
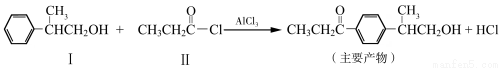
化合物Ⅱ可由化合物Ⅲ合成:
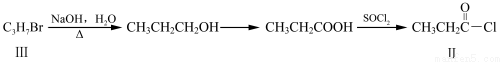
(1)化合物Ⅰ的分子式为 。反应①的反应类型为 。
(2)过量的化合物Ⅰ与HOOCCH2CH2COOH发生酯化反应,反应的化学方程式为
____________________(注明条件)。
(3)化合物Ⅲ的结构简式为 。化合物Ⅲ可与NaOH乙醇溶液共热,反应的化学方程式 _________________________________。
(4)化合物Ⅰ在一定条件下氧化生成化合物Ⅳ(分子式为C9H10O),化合物Ⅳ的一种同分异构体Ⅴ能发生银镜反应,Ⅴ的核磁共振氢谱除苯环峰外还有三组峰,峰面积之比为为2:2:1,Ⅴ的结构简式为 ______________________________
(5)一定条件下,1分子 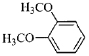 与1分子
与1分子  也可以发生类似反
也可以发生类似反
应①的反应,有机化合物结构简式为______________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com