
| A. | 工业上将NH3与CO2在高温高压下制成[CO(NH2)2] | |
| B. | 空气中的O2和N2在闪电时化合成NO | |
| C. | 豆科植物的根瘤菌把氮气变为NH3 | |
| D. | 工业上用N2和H2来合成NH3 |
分析 元素以单质形态存在则为游离态;元素以化合物形态存在则为化合态.氮的固定是指由游离态的氮转化为化合态的氮,据此解答.
解答 解:A.工业上将NH3与CO2在高温高压下制成[CO(NH2)2],是化合态的氮之间的转化,不属于氮的固定,故A选;
B.空气中的O2和N2在闪电时化合成NO,由游离态的氮转化为化合态的氮,符合氮的固定,属于氮的固定,故B不选;
C.豆科植物的根瘤菌把氮气变为NH3,由游离态的氮转化为化合态的氮,符合氮的固定,属于氮的固定,故C不选;
D.工业上用N2和H2来合成NH3,由游离态的氮转化为化合态的氮,符合氮的固定,属于氮的固定,故D不选;
故选:A.
点评 本题考查了氮的固定,根据固氮的定义可以判断,题目难度不大.


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:选择题

| A. | 据图可知,阳极反应式为2SO42--4e-=2SO3↑+O2↑ | |
| B. | 阳极失去2mol电子时,理论上可以得到11.2L氧气 | |
| C. | SO2在阴极与O2反应生成硫酸根,则方程式为SO2+O2+2e-=SO42- | |
| D. | CO2不参与电极反应,净化器中CO2浓度升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
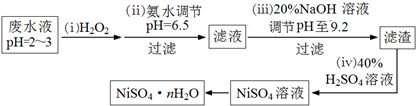
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜分别溶于盐酸和醋酸 | |
| B. | 石灰石分别与硝酸和盐酸反应 | |
| C. | 硫酸铜溶液分别与氯化钡和氢氧化钡溶液反应 | |
| D. | 稀硫酸分别与碳酸钠、碳酸氢钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1.0 mol•L-1CH3COONa溶液中含有CH3COO-的个数为NA | |
| B. | 1.0 L 1.0 mol•L-1NaAlO2溶液中含有的铝原子数为NA | |
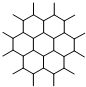
| C. | 如图是石墨晶体结构的俯视图,含1 mol C的石墨中六元环个数为$\frac{{N}_{A}}{2}$ | |
| D. | 22.4 L N2中所含的σ键数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
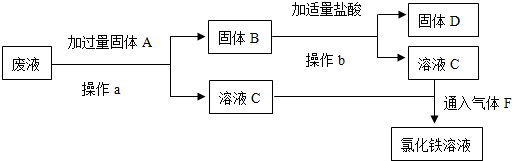
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 分子 | 立体结构 | 杂化方式 | |
| A | 三氧化硫(SO3) | 正三角形 | S原子采用sp杂化 |
| B | 二氧化硫(SO2) | V型 | S原子采用sp3杂化 |
| C | 碳酸根离子(CO32-) | 三角锥型 | C原子采用sp2杂化 |
| D | 乙炔(C2H2) | 直线型 | C原子采用sp杂化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的立体结构模型 | B. | PH3的立体结构模型 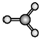 | ||
| C. | H2S的立体结构模型 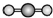 | D. | CH4的立体结构模型 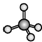 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com