
| A.钢铁在潮湿的空气中比在干燥空气中更容易生锈 |
| B.用加热蒸干AlCl3溶液的方法不能制得无水AlCl3 |
| C.蒸馏水和0.1 mol?L-1 NaOH溶液中的c(H+),前者大于后者 |
| D.向含有少量Fe3+的MgCl2酸性溶液中加入MgCO3,可将Fe3+转化成Fe(OH)3除去 |
 Al(OH)3 + 3H+,用加热蒸干促进水解,盐酸易挥发,生成氢氧化铝沉淀,能用平衡移动原理解释,错误;C、根据H2O
Al(OH)3 + 3H+,用加热蒸干促进水解,盐酸易挥发,生成氢氧化铝沉淀,能用平衡移动原理解释,错误;C、根据H2O  H+ + OH-知,碱抑制水的电离,蒸馏水和0.1 mol?L-1 NaOH溶液中的c(H+),前者大于后者,能用平衡移动原理解释,错误;D、向含有少量Fe3+的MgCl2酸性溶液中存在平衡:Fe3+ + 3H2O
H+ + OH-知,碱抑制水的电离,蒸馏水和0.1 mol?L-1 NaOH溶液中的c(H+),前者大于后者,能用平衡移动原理解释,错误;D、向含有少量Fe3+的MgCl2酸性溶液中存在平衡:Fe3+ + 3H2O  Fe(OH)3 + 3H+,加入MgCO3,氢离子与之反应,平衡正向移动,可将Fe3+转化成Fe(OH)3除去,能用平衡移动原理解释,错误。
Fe(OH)3 + 3H+,加入MgCO3,氢离子与之反应,平衡正向移动,可将Fe3+转化成Fe(OH)3除去,能用平衡移动原理解释,错误。

科目:高中化学 来源:不详 题型:单选题
| A.-183kJ/mol | B.-91.5kJ/mol |
| C.+183kJ/mol | D.+91.5kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.v(A)=0.5mol?L-1?s-1 | B.v(B)=0.3mol?L-1?s-1 |
| C.v(C)=2.0mol?L-1?min-1 | D.v(D)=10mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 HBr+HBrO,下列措施,不能使溶液颜色变浅的是
HBr+HBrO,下列措施,不能使溶液颜色变浅的是 | A.通入乙烯气体 | B.通入SO2气体 | C.加入NaF晶体 | D.加入NaI晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率; |
| C.过氧化氢分解加二氧化锰作催化剂,使单位时间内产生的氧气的量多。 |
| D.久制的氯水PH值变小。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(气)达到平衡的标志是( )
2C(气)达到平衡的标志是( ) 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3 + Q,下列叙述中正确的
2NH3 + Q,下列叙述中正确的 | A.反应物和生成物的浓度相等 | B.反应物和生成物的浓度不再变化 |
| C.降低温度,平衡混合物中NH3的浓度减小 | D.增大压强,不利于氨的合成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 化学方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| I | Fe(s)+CO2(g) 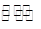 2 FeO(s)+CO(g) 2 FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| II | CO(g)+H2O(g) 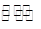 CO2(g)+H2(g) CO2(g)+H2(g) | K2 | 1.62 | b |
| III | Fe(s)+H2O(g)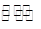 FeO(s)+H2(g) FeO(s)+H2(g) | K3 | a | 1.68 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

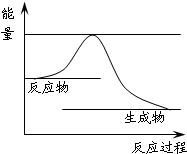

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com