
 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.| 实验序号 | 样品质量/g | CO2体积/mL(已折算成标准状况下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
分析 (1)①用研钵分别研细后再混合研磨,发生水解反应,有CO2气体生成,产生大量气泡,有“磁磁”的声音;
②根据SO42-的检验方法:先加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-;
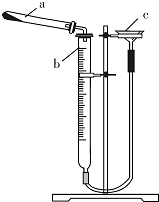
(2))①根据常见仪器的结构写出名称;
②此装置漏斗与大气相通,要进行其气密性检查,首先要考虑的问题是如何使试管不直接通过量气管与大气相通,要解决这一问题,显而易见的用水(或液体)做液封,从而实现这一目的;
③先判断三次平行实验数据的有效性,然后求出平均值,然后根据方程式mCu(OH)2•nCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(m+n)CuO+mH2O+nCO2↑求出$\frac{m}{n}$的值;若量气管中所盛液体为水,二氧化碳溶于水,n值偏小,则m值偏大.
解答 解:(1)①用研钵分别研细后再混合研磨,发生水解反应,有CO2气体生成,产生大量气泡,所以会有“磁磁”的声音,故答案为:有气体生成;
②滤液中是否含有SO42-的操作方法是:取最后一次洗涤液于试管中,先加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-,否则没有,故答案为:取最后一次洗涤液少许于试管中,加入适量盐酸酸化后滴加氯化钡溶液,若无沉淀生成,则没有SO42-,否则含有SO42-;
(2)①仪器b的名称是碱式滴定管,故答案为:碱式滴定管;
②此装置漏斗与大气相通,要进行其气密性检查,首先要考虑的问题是如何使试管不直接通过量气管与大气相通,具体方法:连接好装置,通过漏斗向装置中加水,至漏斗中水面比量气管中高,静置,水面不发生变化则装置不漏气,否则装置漏气,故答案为:连接好装置,通过漏斗向装置中加水,至右侧水面比左侧水面高,静置,水面高度差不发生变化,则装置不漏气,否则装置漏气;
③三次平行实验数据均有效,CO2体积的平均值$\frac{44.82+44.78+44.80}{3}$mL=44.80mL,物质的量为$\frac{0.0448L}{22.4L/mol}$=0.002mol,
mCu(OH)2•nCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(m+n)CuO+mH2O+nCO2
(98m+124n)g nmol
0.542g 0.002mol
$\frac{98m+124n}{0.542}$=$\frac{n}{0.002}$解得:m:n=3:2;
若量气管中所盛液体为水,二氧化碳溶于水,n值偏小,则m值偏大,m与n的比值偏大;
故答案为:3:2;偏大.,故答案为:3:2;偏大.
点评 本题考查物质的制备与组成测定,侧重对实验现象的分析、问题讨论的考查,综合考查学生对知识的迁移应用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 肯定有KNO3和Na2CO3,没有Ba(NO3)2 | |
| B. | 肯定有KNO3,没有Ba(NO3)2,可能还有Na2CO3 | |
| C. | 肯定没有Na2CO3和Ba(NO3)2,可能有KNO3 | |
| D. | 以上判断都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,48gO3中所含的氧原子数为3NA | |
| B. | 1.8gNH4+中所含质子数为0.1NA | |
| C. | 标况下,11.2L氧气中所含原子数为0.5NA | |
| D. | 2.4g金属镁变成离子时得到的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①③⑥ | C. | ②③ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子数:17gOH-与1mol-OH | |
| B. | 双键数目:1mol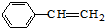 与4mol C2H4 与4mol C2H4 | |
| C. | 分子数:常温常压下16g氧气与4g氦气 | |
| D. | 阴离子总数:72gCaO2与62g Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
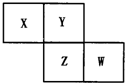 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A. | Z的单质与氢气反应较Y剧烈 | |
| B. | X、Y形成的化合物都易溶于水 | |
| C. | 只由这四种元素不能组成有机化合物 | |
| D. | 最高价氧化物对应水化物的酸性W比Z弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③ | C. | ①③④ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com