
 )
) 2NH3(g) ��H=��92.4kJ/mol
2NH3(g) ��H=��92.4kJ/mol

 2NH3(g)��Ӱ�죮ʵ������ͼ��ʾ��(ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ���)
2NH3(g)��Ӱ�죮ʵ������ͼ��ʾ��(ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ���) �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2C(g)
2C(g)
 2C(g)������N�дﵽƽ�⣬��������к���A 1.0mol��B 0.4mol��C 0.4mol����ʱ�ݻ�Ϊ2.0L����������µ�ƽ�ⳣ��Ϊ �������¶Ⱥ�ѹǿ���䣬���������ͨ��0.36mol A��ƽ�⽫ ������������������ƶ����ü�Ҫ�ļ������˵������
2C(g)������N�дﵽƽ�⣬��������к���A 1.0mol��B 0.4mol��C 0.4mol����ʱ�ݻ�Ϊ2.0L����������µ�ƽ�ⳣ��Ϊ �������¶Ⱥ�ѹǿ���䣬���������ͨ��0.36mol A��ƽ�⽫ ������������������ƶ����ü�Ҫ�ļ������˵������ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ı�����������ܸı仯ѧ��Ӧ���� |
| B����ij��Ӧ��һ�������´ﵽ��Ӧ��ʱ���ﵽ�˻�ѧƽ��״̬ |
| C����ij��Ӧ��ϵ������ѹǿ���ٸı�ʱ���÷�Ӧһ���ﵽ��Ӧ�� |
| D����ij��Ӧ�ﵽ��ʱ����Ӧ����������Ũ��һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
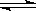 2 NH3��һ�������´ﵽ��ѧ��Ӧ����ʱ�������ж���ȷ����
2 NH3��һ�������´ﵽ��ѧ��Ӧ����ʱ�������ж���ȷ����| A��N2��ȫת��ΪNH3 |
| B����Ӧ������У�NH3�������������ٸı� |
| C��N2��H2��NH3�����ʵ���֮��Ϊ1��3��2 |
| D������1 mol N2��ͬʱ����2 mol NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
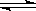 2NH3(g)�ﵽ��ѧƽ��״̬�ı�־��( )
2NH3(g)�ﵽ��ѧƽ��״̬�ı�־��( )| A��N2��H2��NH3�����ʵ���Ũ�Ȳ��ٸı� |
| B��c(N2)��c(H2)��c(NH3)��1��3��2 |
| C��N2��H2�����ʵ���֮����NH3�����ʵ���2�� |
| D��NH3���������ʵ���H2�ķֽ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)+D(g) �Ѵﵽ��Ӧ�ȵ���
C(g)+D(g) �Ѵﵽ��Ӧ�ȵ���| A�����������ܶȱ��ֲ��� | B���У�mol C���ɵ�ͬʱ�У�mol D���� |
| C���������������ʵ������ֲ��� | D����1 mol A���ɵ�ͬʱ�У�mol C���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Z(g)+2W(g)����ƽ��ʱ��A�����Ϊ1.2 a L ������˵����ȷ����
Z(g)+2W(g)����ƽ��ʱ��A�����Ϊ1.2 a L ������˵����ȷ����
 ��v(A)
��v(A)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 bZ(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�����˵����ȷ���ǣ� ��
bZ(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�����˵����ȷ���ǣ� ��
 0��10min�����������ѹǿ������
0��10min�����������ѹǿ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

A���÷�Ӧ�ķ���ʽΪ2NO2 N2O4 N2O4 |
| B��80sǰ�÷�Ӧһ��û�дﵽƽ��״̬ |
| C��a��ȡֵΪ0.56 |
| D��20s��40s����N2O4��ʾ�ķ�Ӧ����Ϊ0.010mol��L-1��S-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com