
【题目】氯化亚砜(SOCl2)是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生。实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示。


(1)实验室制取SOCl2在三颈烧瓶中进行,整个装置所选仪器的连接顺序是⑥→___→①;___→②(已知①处通入Cl2、除杂装置可以重复使用)。
(2)冷凝管上连接的干燥管的作用是:①尾气处理;②___。
(3)实验室制Cl2的离子方程式为___。
(4)该实验中制取SO2,下列最适宜的试剂是___(填下列字母编号)。
A.Cu固体与18.4molL-1硫酸
B.Na2SO3固体与20%硫酸
C.Na2SO3固体与70%硫酸
D.Na2SO3固体与18.4molL-1硫酸
(5)预测SOCl2遇水反应的化学方程式为___。
(6)取少量的SOCl2加入足量NaOH溶液,振荡、静置得到无色溶液,检验溶液中存在Cl-的试剂有____。
【答案】→→⑨→⑩ ⑦→⑨→⑩ 防止空气中的水蒸气进入反应装置而使SOCl2水解 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O C SOCl2+H2O=SO2↑+2HCl Ba(NO3)2、稀HNO3、AgNO3
Mn2++Cl2↑+2H2O C SOCl2+H2O=SO2↑+2HCl Ba(NO3)2、稀HNO3、AgNO3
【解析】
(1)根据方程式SO2+Cl2+SCl2=2SOCl2可知,SO2、Cl2、SCl2反应生成SOCl2,实验室用二氧化锰、浓盐酸制取氯气,用饱和食盐水除去氯化氢、用浓硫酸干燥后通入三口烧瓶;亚硫酸钠固体和浓硫酸反应制取二氧化硫,用浓硫酸干燥后通入三口烧瓶,注意洗气瓶长进短出;
(2)根据SOCl2遇水剧烈反应分析;
(3)二氧化锰、浓盐酸加热生成氯化锰、氯气、水;
(4)根据强酸制弱酸分析;
(5)SOCl2遇水反应,产生白雾说明生成了氯化氢,有刺激性气味的气体产生说明生成二氧化硫气体;
(6)取少量的SOCl2加入足量NaOH溶液,振荡、静止得到无色溶液,溶液中含亚硫酸根离子和氯离子,检验氯离子可用硝酸和硝酸银溶液。
(1)根据方程式SO2+Cl2+SCl2=2SOCl2可知,SO2、Cl2、SCl2反应生成SOCl2,实验室用二氧化锰、浓盐酸制取氯气,用饱和食盐水除去氯化氢、用浓硫酸干燥后通入三口烧瓶;亚硫酸钠固体和浓硫酸反应制取二氧化硫,用浓硫酸干燥后通入三口烧瓶,洗气瓶长进短出,所以整个装置所选仪器的连接顺序是⑥→→→⑨→⑩→①;⑦→⑨→⑩→②;
(2)SOCl2遇水剧烈水解,冷凝管上连接的干燥管,可以防止空气中的水蒸气进入反应装置使SOCl2遇水水解;
(3)二氧化锰、浓盐酸加热生成氯化锰、氯气、水,反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(4)A.Cu固体与18.4molL-1硫酸,能放出二氧化硫,消耗的硫酸多,故不选A;
B.Na2SO3固体与20%硫酸,硫酸浓度太小,因SO2的溶解度较大,放出二氧化硫的量少,故不选B;
C.Na2SO3固体与70%硫酸,硫酸浓度适合,反应生成二氧化硫气体,故选C;
D. 18.4molL-1硫酸中氢离子浓度很小,Na2SO3固体与18.4molL-1硫酸不能制备二氧化硫气体,故不选D;
(5)SOCl2遇水反应,成了氯化氢和二氧化硫,反应的化学方程式是SOCl2+H2O=SO2↑+2HCl;
(6)取少量的SOCl2加入足量NaOH溶液,振荡、静止得到无色溶液,含亚硫酸根离子和氯离子,检验溶液存在的Cl-的方法是取少量溶液于试管中,加入过量Ba(NO3)2溶液,静置,取上层清液,滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Cl-。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O32﹣+O2+xOH﹣=Fe3O4+S4O62﹣+2H2O,下列说法中不正确的是
A. 每生成1mol Fe3O4,反应转移的电子总数为4mol
B. Fe2+和S2O32﹣都是还原剂
C. x=4
D. 1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.1molFe分别与1molCl2、1molS充分反应,转移的电子数比为3:2
B.80mL10mol/L浓盐酸与过量MnO2加热反应,生成的Cl2分子数为0.2NA
C.标准状况下,22.4mLSO3中含有的硫、氧原子个数比为1:3
D.100g63%的HNO3溶液中含有的氧原子个数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为中学化学中常见物质,一定条件下它们之间有如下转化关系(其它产物已略去):下列说法不正确的是
![]()
A. 若W是单质铁,则Z溶液可能是FeCl2溶液
B. 若W是氢氧化钠,则X水溶液呈酸性
C. 若W是氧气,则X、Z的相对分子质量可能相差48
D. 若W是强氧化性的单质,则X可能是金属铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组探究甲烷与氯气的取代反应,装置、现象如下:
现象 |
ⅰ.光照后,产生白雾,混合气体颜色变浅 ⅱ.试管内液面上升至试管的2/3;试管壁和液面上出现少量油状液滴 |

下列说法不正确的是
A. 饱和食盐水可以减少氯气的溶解
B. 油状液滴的主要成分是一氯甲烷
C. 产生白雾以及试管内液面上升证明有氯化氢生成
D. 为了探究反应条件,可用黑色纸套套住装满甲烷和氯气的试管,一段时间后进行观察
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-氰基烯酸酯类医用胶无毒无害、性质稳定、与生物组织粘合好,可用做手术伤口粘合剂。其分子结构可用如图所示的通式表示:

资料卡片:
①分子中 “—R1”部分碳链适当增长,有助于延长固化时间。
②分子中 “-R2”部分碳链增长,耐水性增强,更适合在水湿环境中粘合。
③分子中 “-R2”部分若再引入一个α-氰基烯酸酯的结构,则可发生交联聚合,使胶膜硬度、韧性均增强。
(1)502胶是应用最早的医用胶,主要成分是![]() 。
。
① 该分子中含有的官能团是氰基(—CN)、碳碳双键和_______。
② 该物质具有粘合性的原因是发生加聚反应(微量水蒸气作用下),化学方程式是_______。
③ 常温下,丙烯难以聚合,而502胶可以快速聚合。从分子结构的角度分析产生该差异的原因是_______。
(2)科学家已将502胶改良为504胶(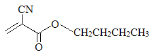 ),504胶相对502胶的优点是_______。
),504胶相对502胶的优点是_______。
(3)用于粘接骨骼的“接骨胶”固化时间不能太短,且粘合后强度要高。请设计一种 “接骨胶”,写出其主要成分的结构简式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EPR橡胶(聚乙丙烯)和工程材料聚碳酸酯(简称PC)的一种合成路线如下:

已知:酯与含羟基的化合物可发生如下酯交换反应:RCOOR’+R”OH![]() RCOOR”+R’OH
RCOOR”+R’OH
请回答:
(1)D中所含的官能团是_______。
(2)EPR橡胶的结构简式_______。
(3)下列说法正确的是_______(填字母)。
a.反应③的原子利用率为100%
b.反应④为取代反应
c.1mol F与足量金属Na反应,最多可生成22.4L H2(标准状况下)
(4)反应②的化学方程式是_______。
(5)反应②生成E时会产生多种副产物,其中有一种分子式为C9H12O2的副产物M,其结构简式为_______。
(6)反应⑤的化学方程式是_______。
(7)已知: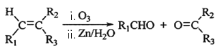 (R1、R2、R3代表烃基)写出以D为原料合成己二酸[HOOC(CH2)4COOH]的合成路线,无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件_______________________。
(R1、R2、R3代表烃基)写出以D为原料合成己二酸[HOOC(CH2)4COOH]的合成路线,无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件_______________________。
示例:CH3CH2OH![]() CH2=CH2
CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有X(g)+Y(g) ![]() 2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据图回答:从t2→t3的曲线变化是由哪种条件引起的
2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据图回答:从t2→t3的曲线变化是由哪种条件引起的

A. 增大X或Y的浓度 B. 增大压强
C. 增大Z的浓度 D. 升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的原因的是
A. 铜久置空气中表面出现绿色固体:2Cu+O2+CO2+H2O═Cu2(OH)2CO3
B. 某种火箭发射阶段有少量N2O4,逸出,产生红色气体:N2O4![]() 2NO2
2NO2
C. FeSO4·7H2O在空气中久置变黄:2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O
Fe2O3+SO2↑+SO3↑+14H2O
D. SO2通入KMnO4溶液中,溶液紫色逐渐褪去:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4十2H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com