
 O2(g)=H2O(l)△H=-285.8kJ?mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1
O2(g)=H2O(l)△H=-285.8kJ?mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1 kJ/mol=648.5kJ/mol,根据十字交叉法计算原混合气体中H2和CH4的物质的量之比.
kJ/mol=648.5kJ/mol,根据十字交叉法计算原混合气体中H2和CH4的物质的量之比. =5mol,
=5mol, kJ/mol=648.5kJ/mol,
kJ/mol=648.5kJ/mol, O2(g)=H2O(1)△H=-285.8kJ?mol-1可知,氢气的燃烧热为285.8kJ/mol;
O2(g)=H2O(1)△H=-285.8kJ?mol-1可知,氢气的燃烧热为285.8kJ/mol;


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
 已知:H2(g)+
已知:H2(g)+| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 2 |
- 6 |
+ 2 |
- 6 |
+ 4 |
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:
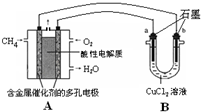 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.| 1 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省江门市高三调研测试理综化学试卷(解析版) 题型:填空题
对大气污染物SO2、NOx进行研究具有重要环保意义。请回答下列问题:
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。
已知:H2(g)+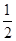 O2(g)=H2 O(g) △H=-241.8kJ·mol-1
O2(g)=H2 O(g) △H=-241.8kJ·mol-1
C(s)+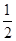 O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式: 。
(2)已知汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g)
△H
2NO(g)
△H 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在1.0 L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4 mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在1.0 L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4 mol。
①5s内该反应的平均速率ν(NO) = (保留2位有效数字);在1300oC 时,该反应的平
衡常数表达式K= 。
②汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
(3)汽车尾气中NO和CO的转化。当催化剂质量一定时,增大催化剂固体的表面积可提高化学反应速率。右图表示在其他条件不变时,反应2NO(g)+2CO(g)
 2CO2(g)+N2(g) 中,NO的浓度
2CO2(g)+N2(g) 中,NO的浓度
c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。

①该反应的△H 0 (填“>”或“<”)。
②若催化剂的表面积S1>S2,在右图中画出c(NO) 在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com