
【题目】[化学——选修5:有机化学基础]
苯酚是一种重要的化工原料。以苯酚为主要起始原料,某种药物中间体的合成路线如下:

已知:![]()
(1)C中含氧官能团的名称为 ;
(2)反应I的反应类型是 ;
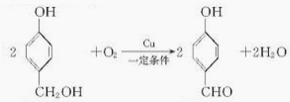
(3)反应Ⅱ的化学方程式为 ;
(4)化合物B的名称是 ,E的结构简式为 ;
(5)写出满足下列条件的F的同分异构体的结构简式 (任写两种)。
![]() ①苯环上有三个取代基且苯环上的一氯取代物只有两种.②能与FeCl3溶液发生显色反应.③红外光谱显示有
①苯环上有三个取代基且苯环上的一氯取代物只有两种.②能与FeCl3溶液发生显色反应.③红外光谱显示有
【答案】(1)醛基、酚羟基
(2) 加成反应
(3)
(4)乙醛;![]()
(5)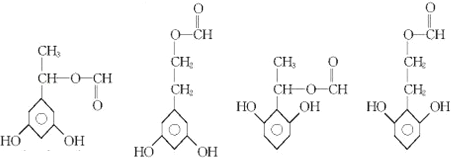 (任意2个)
(任意2个)
【解析】
试题分析:苯酚与甲醛发生加成反应生成 ,
, 发生催化氧化生成A为
发生催化氧化生成A为![]() ,由C的结构简式、结合给予的信息可知B为CH3CHO,C发生银镜反应、酸化得到D为
,由C的结构简式、结合给予的信息可知B为CH3CHO,C发生银镜反应、酸化得到D为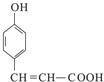 ,D与HBr发生加成反应生成E,E发生水解反应、酸化得到F,F发生酯化反应生成M,结合M的结构简式可知,E为
,D与HBr发生加成反应生成E,E发生水解反应、酸化得到F,F发生酯化反应生成M,结合M的结构简式可知,E为![]() ,F为
,F为![]() 。
。
(1)由C的结构简式可知,C中含氧官能团的名称为:醛基、酚羟基。
故答案为:醛基、酚羟基;
(2)反应I的反应类型是:加成反应。
故答案为:加成反应;
(3)反应Ⅱ的化学方程式为: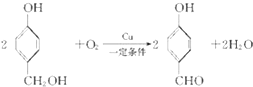 。
。
故答案为: ;
;
(4)B为CH3CHO,名称是乙醛,E的结构简式为:![]() 。
。
故答案为:乙醛;![]() ;
;
(5)F(![]() )的同分异构体下列满足:①苯环上有三个取代基且苯环上的一
)的同分异构体下列满足:①苯环上有三个取代基且苯环上的一
氯取代物只有两种,有2个相同的取代基,且为对称结构,②能与FeCl3溶液发生显色反应,说明含有酚羟基,③红外光谱显示有![]() ,可能的结构简式为:
,可能的结构简式为:
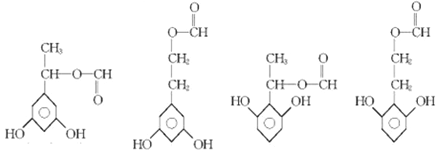 。
。
故答案为: 任意2种。
任意2种。


科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾晶体(K3[Fe(C2O4) 3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+。
重复步骤二、步骤三操作,滴定消耗0.010mol/LKMnO4溶液19.98ml。
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作步骤依次是:称量、 、转移、洗涤并转移、 摇匀。
②加入锌粉的目的是 。
③写出步骤三中发生反应的离子方程式 。
④实验测得该晶体中铁的质量分数为 。在步骤二中,若加入的KMnO4溶液的量不够,则测得的铁含量 。(选填“偏低”“偏高”“不变”)
(2)结晶水的测定
将坩埚洗净,烘干至恒重,记录质量;在坩锅中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,置于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误: ; 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃ Ksp(Ag2S)=6.3×10-50、Ksp(AgCl)=1.5×10-16。沙市中学某研究性学习小组探究
AgCl、Ag2S沉淀转化的原因。
步 骤 | 现 象 |
Ⅰ.将NaCl与AgNO3溶液混合 | 产生白色沉淀 |
Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
Ⅲ.滤出黑色沉淀,加入NaCl溶液 | 较长时间后,沉淀变为乳白色 |
(1)Ⅰ中的白色沉淀是 。
(2)Ⅱ中能说明沉淀变黑的的离子方程式是 ,沉淀转化的主要原因是 。
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl。用浓HNO3溶解,产生红棕色气体,部分沉淀未溶
解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y中滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是 。
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀_____ _。
(4)该学生通过如下对照实验确认了步骤Ⅲ中 乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化。

现 象 | B:一段时间后,出现乳白色沉淀 |
C:一段时间后,无明显变化 |
①A中产生的气体是_________。
②C中盛放的物质W是_________。
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S + ![]() +
+ ![]() + 2H2O
+ 2H2O ![]() 4AgCl +
4AgCl + ![]() + 4NaOH
+ 4NaOH
④从平衡移动的角度,解释B中NaCl的作用: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

(1)装置A中盛放亚硫酸钠的仪器名称是_____,其中发生反应的化学方程式为_____。
(2)实验过程中,装置B、C中发生的现象分别是____________、______________,这些现象分别说明SO2具有的性质是____和__;装置B中发生反应的离子方程式为__________。
(3)设计装置D的目的是____________________________________________________。
(4)尾气应用____________________溶液吸收(填试剂的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中加入2.0 mol SO2和1.0 mol O2,一定条件下发生如下反应2SO2+ O2![]() 2SO3。反应达到平衡后,各物质的物质的量可能为
2SO3。反应达到平衡后,各物质的物质的量可能为
n(SO2)/mol | n(O2)/mol | n(SO3)/mol | |
A | 1.0 | 0 | 1.0 |
B | 0 | 0 | 2.0 |
C | 0.2 | 0.1 | 1.8 |
D | 1.5 | 0.75 | 1.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2·xH2O是用途广泛的基础化工产品。我国目前主要是用盐酸和硫化钡(含少量Mg2+、Fe3+等)反应生产BaCl2·xH2O,工艺流程如下图所示。

已知:室温时Ksp[Mg(OH)2]=1.8×10-11 , Ksp[Fe(OH)3]=4.0×10-38 ,请回答下列问题:
(1)反应Ⅰ中生成的H2S用足量氨水吸收,一定条件下向所得溶液中通入空气,又可得到单质硫并使吸收液再生,再生反应的化学方程式为_____________________________________。
(2)所得氯化钡粗液中含硫化合物(H2S、HS-等)影响产品质量,可鼓入预热后的空气吹除,预热空气的目的是_______________;沉淀A的主要成分是_______________。
(3)热空气吹除时会有部分HS-转变为S2O O32-,使产品仍达不到纯度要求,可再进行酸化脱硫,酸化脱硫时的离子方程式为______________________________________________________。
(4)室温时,若加碱调溶液pH调至9,则完全沉淀的离子是__________,另一离子浓度为______mol/L (当溶液中离子浓度小于1×10-5 mol/L时认为该离子完全沉淀) 。若向0.1 mol/L FeCl3溶液中加入一定量等浓度的Na2CO3溶液,出现的现象________,发生反应的离子方程式___________________。
(5)将足量的SO2气体通入BaCl2溶液中有无明显现象_____________(填“有”或“无”),向NaOH溶液中通入足量的SO2气体,写出所得溶液离子浓度的大小顺序________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N为短周期的第五种主族元素。其中X、Z同主族,Y、Z同周期,M与X、Y既不同主族,也不同周期。X原子最外层电子数是核外电子层数的三倍,Y的最高化合价与其最低化合价的代数和等于6。N是短周期主族元素中原子半径最大的非金属元素。
(1)X元素位于元素周期表的位置是第 周期,第 族
(2)请写出下列反应的离子方程式:N单质与氢氧化钠溶液反应:
(3)Y与Z相比,非金属性较强的元素的原子结构示意图为 ,可以证明该结论的实验是(用离子方程式表示) 。
(4)请将X、Z、M、N元素原子半径从大到小排序: (用元素符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知某烷烃分子中电子数为42。
(1)该烷烃的分子式为________________________。
(2)写出该烷烃分子的所有同分异构体的结构简式:_________________________。
(3)上述同分异构体中,在相同条件下沸点最低的是____________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年8月12日,天津滨海新区爆炸事故确认有氰化钠(NaCN)、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢气体。氰化氢的沸点只有26摄氏度,因此相当容易挥发进入空气,这就大大增加了中毒的风险。同时氰化钠遇到亚硝酸钠会发生爆炸。回答下列问题
(1)写出氰化钠遇水产生氰化氢的离子方程式
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体碳酸氢钠,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式 。
(3)氰化钠遇到亚硝酸钠能生成氧化钠和两种无污染的气体发生爆炸,写出化学反应方程式 。
(4)爆炸残留在废水中的CN- 可以用Cr2O72-处理,拟定下列流程进行废水处理,
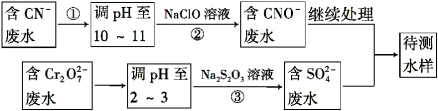
① 上述处理废水流程中主要使用的方法是 ;
A.混凝法 B.中和法 C.沉淀法 D.氧化还原法
② 步骤②反应无气体放出,该反应的离子方程式为_______________________;
③ 步骤③中,每处理0.4 mol Cr2O72 - 时转移电子2.4 mol,该反应的离子方程式为 ___________;
④处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol Cr2O72-,需加入amol FeSO4·7H2O,下列结论正确的是 。
A.x=0.5,a=6 B.x=0.5,a=10 C.x=1.5,a=6 D.x=1.5,a=10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com