
短周期元素的X、Y、Z、W原子序数依次增大,X原子最外层电子数是电子层数的三倍,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比原子Y原子多1,W与X同主族,则
A.气态氢化物的稳定性:X>W
B.单质的还原性:Y>Z
C.原子半径:Y<Z<W
D.Y和Z两者最高价氧化物对应的水化物能相互反应
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源:2015届广东省揭阳市高三上学期第一次阶段考试理综试卷(解析版) 题型:选择题
下列关于金属及其化合物的叙述正确的是
A.Fe与S混合加热生成FeS2
B.过量的Cu与浓硝酸会有NO生成
C.NaHCO3、Na2CO3、MgCO3受热均能分解生成气体
D.Na2O2与水反应、红热的Fe与水蒸气反应均能反应生成碱
查看答案和解析>>
科目:高中化学 来源:2015届广东省增城市毕业班调研测试理科综合化学试卷(解析版) 题型:实验题
(16分)二甲醚是重要的有机中间体,利用二氧化碳加氢合成二甲醚能变废为宝,且可替代汽油作为新型清洁燃料。
(1)常温常压下,二氧化碳加氢可选择性生成二甲醚或一氧化碳:
①CO2 (g)+3H2(g)=CH3OH(l)+H2O(l) △H1 =-55.7 kJ/mol
②2CH3OH(l) = CH3OCH3(g)+H2O (l) △H2 =-23.4 kJ/mol
③CO2 (g)+3H2(g) =CO (g) + H2O (l) △H 3>0
则CO2(g)加氢转化为CH3OCH3(g)和H2O (l)的热化学方程式是___________________________________________________。
(2)合成二甲醚往往选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。下图是硅铝比与产物选择性图:
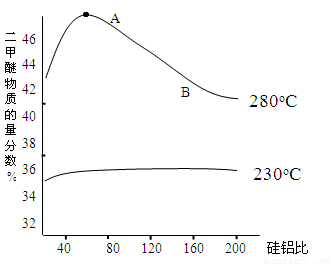
反应③的平衡常数表达式为 ,图中A点和B点的平衡常数比较:KA______KB(填“>、=、<”)。根据以上两条曲线,写出其中一条变化规律: ___________________。
(3)在280oC时,向一个2L的密闭容器中加入等量2mol二氧化碳和氢气, A点二甲醚的浓度为0.15 mol·L-1,计算在A点二氧化碳的转化率,要求写出计算过程。
(4)二甲醚逐渐发展为替代汽油的清洁燃料,在二甲醚燃料电池中,二甲醚通入______极,碱性条件下,该电极反应式是 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三10月月考化学试卷(解析版) 题型:选择题
下列各组物质的无色溶液,不用其它试剂即可鉴别的是
A.NaHCO3 Na2CO3 BaCl2
B.KOH Na2SO4 AlCl3
C.KHCO3 NaHSO4
D.Ca(OH)2 Na2SO3 BaCl2
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:填空题
(10分)汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO、NOx等)的污染是重要的科学研究课题。
(1) 已知:N2(g) + O2(g) 2NO(g) ΔH1
2NO(g) ΔH1
N2(g) + 3H2(g) 2NH3(g) ΔH2
2NH3(g) ΔH2
2H2(g) + O2(g) 2H2O(g) ΔH3
2H2O(g) ΔH3
则4NO(g) + 4NH3(g) + O2(g) 4N2(g) + 6H2O(g) ΔH =____________(用ΔH1、ΔH2、ΔH3表达)
4N2(g) + 6H2O(g) ΔH =____________(用ΔH1、ΔH2、ΔH3表达)
(2) 在密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g),下列说法不能说明该反应达到平衡的是__________ (填字母)
N2(g)+2CO2(g),下列说法不能说明该反应达到平衡的是__________ (填字母)
A.NO的生成速率与NO的消耗速率相等
B.v(CO)=v(CO2)
C.体系的压强保持不变
D.各物质的浓度保持不变
(3) 可用活性炭还原法处理氮氧化物。有关反应的化学方程式为:
C(s) + 2NO(g) N2(g) + CO2(g) ΔH >0
N2(g) + CO2(g) ΔH >0
某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1
| NO | N2 | CO2 |
0
| 0.100
| 0
| 0
|
10
| 0.058
| 0.021
| 0.021
|
20
| 0.040
| 0.030
| 0.030
|
30
| 0.040
| 0.030
| 0.030
|
40
| 0.032
| 0.034
| 0.017
|
① 写出该反应的平衡常数表达式:K= 。
② 30 min后,改变某一条件,平衡发生了移动,则改变的条件是 ;若升高温度,NO浓度将 (填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.将少量的H2S气体通入硫酸铜溶液中: H2S+Cu2+=CuS↓+2H+
B.将NO2气体通入水中:2NO2+H2O= NO3-+ NO↑+2H+
C.ICl 和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-= I-+ ClO-+H2O
D.往100ml 1.5mol/L的FeBr2 溶液中通入0.15mol Cl2:2Br-+Cl2=Br2+2Cl-
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
下列实验“实验操作”与“结论”对应关系正确的是
选项 | 实验操作 | 结论 |
A | 向Fe(NO3)2溶液的试管中加入稀H2SO4 ,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
B | 向沸水中逐滴加入1~2 mL FeCl3饱和溶液,煮沸至红褐色液体 | 制备Fe(OH)3胶体 |
C | 常温下,向饱和 | 说明常温下
|
D | 向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市高三上学期第二次模拟考试化学试卷(解析版) 题型:选择题
下述实验设计能够达到目的的是( )
选项 | 实验目的 | 实验设计 |
A | 证明SO2有漂白性 | 把SO2通入品红溶液中 |
B | 除去Cu粉中的CuO | 向混合物中滴加适量稀硝酸 |
C | 检验溶液中是否含有Fe2+ | 向溶液中滴入KSCN溶液,再滴加氯水 |
D | 证明H2CO3酸性比H2SiO3强 | Na2CO3和SiO2在高温下熔融反应 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省东莞市高三第一次调研考试理科化学试卷(解析版) 题型:选择题
无色透明的酸性溶液中,能大量共存的是
A.Na+、K+、CO32-、NO3- B.K+、Fe2+、NH4+、NO3-
C.NH4+、Al3+、SO42-、NO3- D.K+、Na+、NO3-、OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com