
【题目】如图是配制一定物质的量浓度溶液的过程示意图。下列说法中错误的是( )
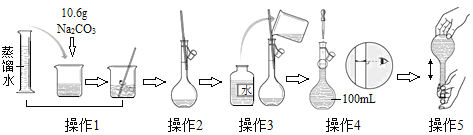
A.所配制的Na2CO3溶液的物质的量浓度为1.0 mol · L-1
B.操作2是将溶解并放置至室温的Na2CO3溶液转移到容量瓶中
C.操作4如果仰视,会使配得溶液的浓度偏低
D.操作5中,定容摇匀后发现液面低于刻度线,继续加水至液面与刻度线相切
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】用1.0mol·L -1NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积(V)关系如右图所示,则原硫酸溶液的物质的量浓度和恰好完全反应后溶液的总体积分别是(设二者混合后体积为二者体积之和)
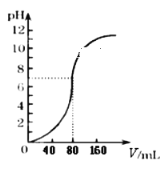
A. 0.5mol·L-1 80mLB. 0.5mol·L-1 160mL
C. 1.0mol·L-1 80mLD. 1.0mol·L-1 160mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中△H的含义表示正确的是
A. H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H(中和热)
B. NaOH(aq)+![]() H2SO4(浓)=
H2SO4(浓)=![]() Na2SO4(aq)+H2O(l) △H(中和热)
Na2SO4(aq)+H2O(l) △H(中和热)
C. CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H(燃烧热)
D. 2H2(g)+O2(g)=2H2O(g) △H(燃烧热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列判断正确的是( )
A.标准状况下,11.2 L H2O 中含有的氧原子数为0.5NA
B.5.6 g铁与足量盐酸反应转移的电子数为0.3NA
C.16 g O2与16 g O3含有的氧原子数目相等
D.常温常压下,11.2 L氯气所含原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式中正确的是
A.向Ca(HCO3)2溶液加入过量的NaOH溶液:![]()
B.向NH4HCO3溶液中滴入少量NaOH溶液:![]()
C.澄清石灰水与少量小苏打溶液混合::![]()
D.少量氢氧化钡溶液与过量硫酸氢钠混合:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)有下列物质:①铜;②石灰水;③CO2;④Fe(OH)3溶液;⑤CaO;⑥豆浆。其中属于胶体的是_____(填序号,下同),属于碱性氧化物的是_____
(2)在标准状况下,35.5g氯气的体积是_____L.将其与氢气化合,需氢气的物质的量是_____mol,将生成的气体溶于水,配成500mL溶液,则该溶液中溶质的物质的量浓度是_____mol/L
(3)如图所示,将充满NO2气体的试管倒扣在水槽中,观察到试管内气体颜色由_____色逐渐变为无色,最终试管内液面上升至试管容积的_____处(填分数)
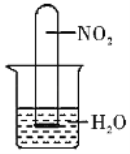
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在人类生产、生活中发挥着重要的作用
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是_____(填化学式,下同),适宜做耐火材料的是_____
(2)若Na2CO3粉末中混有少量 NaHCO3杂质,最适宜的除杂方法是_____,反应的化学方程式_____
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入铁粉,其原因是_____(用离子方程式表示)
(4)Na2O2可用作呼吸面具中的供氧剂写出有关反应的化学方程式_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化学工业基础原料和液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度(℃) | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) | K3 | ||
(1)反应②是_________(填“吸热”或“放热”)反应。
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如下图1所示。则平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”)。
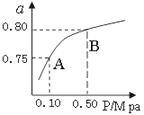
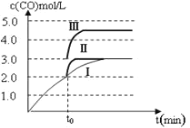
图 1 图2
(3)判断反应③△H____0; △S____0(填“>”“=”或“<”)在500℃、2L的密闭容器中,进行反应③,测得某时刻H2、CO2、 CH3OH、H2O的物质的量分别为6mol、2 mol、10 mol、10 mol, 此时v(正)___v(逆)(填“>”“=”或“<”)
(4)一定温度下,在3 L容积可变的密闭容器中发生反应②,已知 c(CO)与反应时间t变化曲线Ⅰ如上图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_____________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸.常温条件下,将amol/L的CH3COOH与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现以淀粉或乙烯为主要原料都可以合成乙酸乙酯,其合成路线如图所示。

(已知:2CH3CHO+O2![]() 2CH3COOH)
2CH3COOH)
(1)A中含有的官能团名称是______________;其中③的反应类型是______________;
⑥的反应类型是______________;
(2)写乙烯的电子式:_________________乙烯的结构简式:____________;
(3)写出下列反应的化学方程式:①__________________;⑤______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com